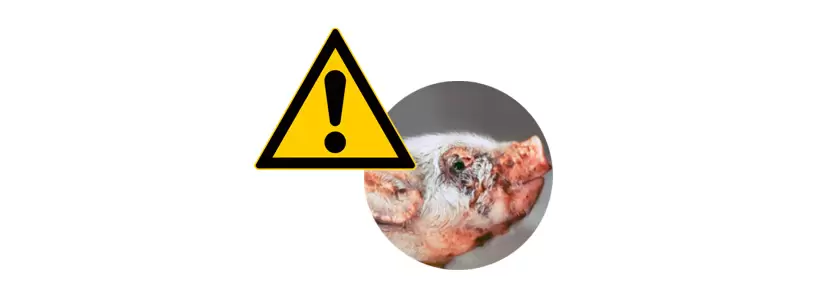
La Epidermitis Exudativa (EE), es una patología dermatológica que en los últimos años, con el crecimiento de las explotaciones y la producción intensiva, hemos visto aumentada su incidencia en nuestras granjas.
Denominada también Eczema húmedo o enfermedad del cerdo graso (greasy pig disease) es fácilmente reconocida por todos por el aspecto tan característico que presentan los lechones (piel de rinoceronte)
Está producida por Staphylococcus hyicus, una bacteria gram positiva que a menudo encontramos en la piel y en el medio ambiente. La enfermedad se desarrolla cuando la bacteria entra al interior de la epidermis a través de heridas. Afecta principalmente a lechones lactantes y a los recién destetados.
La primera fuente de infección es el canal del parto de las cerdas portadoras, donde la bacteria se multiplica profusamente los días precedentes al parto. Posteriormente las heridas, producidas en las peleas al competir por los pezones y en los reagrupamientos, servirán de entrada a la bacteria. Cualquier elemento abrasivo para la piel (suelos rugosos, esquinas afiladas…) constituirá un factor de riesgo para la entrada del Staphylo.
CUADRO CLÍNICO
La denominación de “eczema húmedo” se refiere a los aspectos de la enfermedad visibles en la piel. El eczema suele empezar en las fosas nasales, luego avanza hacia las orejas, cuello, vientre y finalmente se extiende por todo el cuerpo.
Durante las peleas por los mejores pezones las heridas suelen producirse en la cara y las extremidades por mordiscos y arañazos entre hermanos. Es allí donde comienza el problema. La enfermedad se mantiene focalizada si los lechones calostran correctamente y reciben inmunidad de la madre. La aparición de un serotipo nuevo por la entrada de cerdas portadoras o los partos de cerdas jóvenes que no hayan desarrollado inmunidad son factores determinantes, así como la presencia de enfermedades inmunosupresoras (PCV2 y PRRS)
Al principio la piel es húmeda y viscosa. Los lechones están pegajosos al tacto. Más tarde la piel se reseca formando una corteza dura. Los lechones gravemente enfermos están como cubiertos de un caparazón negro, duro y sólido. La patogenicidad viene determinada por una toxina exfoliante que provoca la separación de las células de la epidermis y del estrato espinoso superior, lo que permite una rápida diseminación intradérmica de la bacteria. Se invade masivamente piel, ganglios linfáticos y sangre.
Esta diseminación puede llegar a provocar la deshidratación y muerte septicémica.
“El coste de la EE para la industria porcina en su conjunto no se ha cuantificado y el efecto en las diferentes granjas es muy variable. En cerdos jóvenes, la mortalidad puede llegar a ser del 5% en brotes severos. La disminución del crecimiento en los cerdos afectados puede ser de hasta un 10% a lo largo de su vida, agregando 2 semanas a la edad de sacrificio de estos animales” M. White
DIAGNÓSTICO
El diagnóstico se realiza a partir de las lesiones y síntomas observados y el aislamiento del S.hyicus de las heridas.
También se pueden observar lesiones renales; en la pelvis renal se hallan restos de un precipitado blanco amarillento y pielonefritis.
CONTROL Y TRATAMIENTO
Aunque un tratamiento temprano parenteral con antibióticos de elección (amoxicilina, lincomicina, trimetoprim, sulfamidas) puede ser muy efectivo, se ha observado un aumento de resistencias producidas por S. hyicus, por lo que en casos de persistencia del problema será necesario un estudio de AMR.
Sería recomendable también realizar una tratamiento tópico a los lechones con desinfectantes (yodados o clorhexidina) o antibióticos tópicos en spray. Y se requiere un tratamiento de soporte con electrolitos para paliar la deshidratación, así como suplementos vitamínicos en los casos más graves con lesiones generalizadas.
Pero hay que recordar que la EE es una enfermedad típicamente multifactorial. Pese a que identificar y corregir un sólo factor puede ser suficiente en algunos casos, en muchos continuaremos teniendo problemas.
Otras medidas de control:
-Mejorar la inmunidad maternal así como una correcta adaptación de las nulíparas
-Lavar a las cerdas antes del parto
-Lavar y desinfectar parideras así como las salas de destete
-Asegurar el encalostramiento de los lechones
-En algunas camadas donde se observen muchas peleas, el corte de colmillos preventivo puede ayudar
-Evitar altas humedades
-Evitar suelos y materiales abrasivos, así como productos irritantes para la piel
–Revisar Circovirus y PRRS
Tal como he comentado a lo largo del artículo, todas aquellas enfermedades que provoquen la supresión del sistema inmune, favorecerán el desarrollo de la forma generalizada de la EE. En aquellas explotaciones que se vacune de PCV2, habrá que revisar si la dosis, manejo y pauta vacunal es la adecuada.
Hay varios casos publicados de explotaciones donde la agudización del problema está directamente relacionado con la presencia de Circovirus o/y de PRRS.
-
En Uruguay se realizó un estudio (Ramos et al. 2012), para investigar la presencia de PCV2 en los lechones afectados de EE. Se aprovechó además para analizar las relaciones filogenéticas de las cepas aisladas. En junio de 2011 se informó de un brote de EE , los sueros de animales afectados y sanos fueron analizados para detectar la presencia de circovirus. Exclusivamente, en los lechones enfermos encontraron PCV2. El análisis filogenético mostró que los aislamientos de PCV2 pertenecían al genotipo PCV2b, primera vez detectado en Uruguay.
-
Un brote de EE entre los lechones de una explotación SPF sueca inició un estudio para descubrir las posibles causas del brote.(Wattrang et al, 2002). El estudio incluyó muestras de suero de la explotación SPF en un período de 10 años y se realizó un seguimiento exhaustivo de los animales de la explotación durante un tiempo posterior al brote. También se incluyeron muestras de suero de los machos que proveían de semen a la explotación. La serología del PVC-2 demostró que los animales de la explotación eran seronegativos por lo menos hasta 2 meses antes del brote de EE. Durante el período posterior al brote, los animales mostraron niveles variables de anticuerpos frente a PCV-2, pero todos los animales seroconvertieron positivamente 4 meses después. Los verracos también fueron seropositivos a PCV-2 en el momento del brote.