Para leer más contenidos de Revista porciSapiens Abril 2023
Para leer más contenidos de Revista porciSapiens Abril 2023
| El Síndrome Respiratorio y Reproductivo Porcino (PRRS), cuyo agente etiológico es un virus (PRRSv), es una de las enfermedades del ganado porcino que mayores pérdidas económicas ocasiona, siendo de muy difícil control en los sistemas de producción actuales.
Hoy en día, en algunos países no solo se está trabajando en el control de la enfermedad a nivel de granja, sino que se está apostando por el control regional del virus e incluso se han llegado a implementar planes de erradicación de la enfermedad a nivel nacional que incluyen la combinación de estrategias de bioseguridad, manejo (Sistema McRebel) y protocolos de vacunación. |
LA VACUNACIÓN REDUCE LA CIRCULACIÓN DEL PRRSV EN GRANJAS INFECTADAS Y DISMINUYE LA CLÍNICA ASOCIADA A LA ENFERMEDAD
En los últimos años, para el control y erradicación del PRRSv se han utilizado diversas estrategias, entre ellas, los protocolos de vacunación mixtos.

EL USO DE VACUNAS INACTIVADAS PROPORCIONA MAYOR SEGURIDAD A PRODUCTORES Y VETERINARIOS AL NO INTRODUCIR MÁS CEPAS VIVAS DEL VIRUS EN LA GRANJA CON POSIBILIDAD DE RECOMBINAR CON LAS CEPAS PRESENTES EN LA MISMA
| En este artículo se exponen los resultados de dos nuevos estudios de campo publicados en 2022. 1 El primer estudio (Martin-Valls y cols.) valora los resultados reproductivos y la inmunidad frente a PRRSv en lechones descendientes de cerdas vacunadas con dos protocolos vacunales distintos que incluyen o no una KV (Progressis®). 2 El segundo trabajo expuesto (Pertich y cols.) describe las acciones llevadas a cabo en una granja y los resultados de estas para la erradicación de PRRSv, iniciando el proceso utilizando una KV (Progressis®). |

EXPERIENCIA DE CAMPO Nº 1
RESULTADOS REPRODUCTIVOS E INMUNIDAD
DISEÑO EXPERIMENTAL
Este estudio se llevó a cabo en dos granjas, ambas en una situación de inestabilidad frente al PRRS, con producción de lechón de 6-7 kg:
| GRANJA 1 300 reproductoras y manejo en bandas cada tres semanas. |
GRANJA 2 1.700 reproductoras y manejo en bandas semanales. |

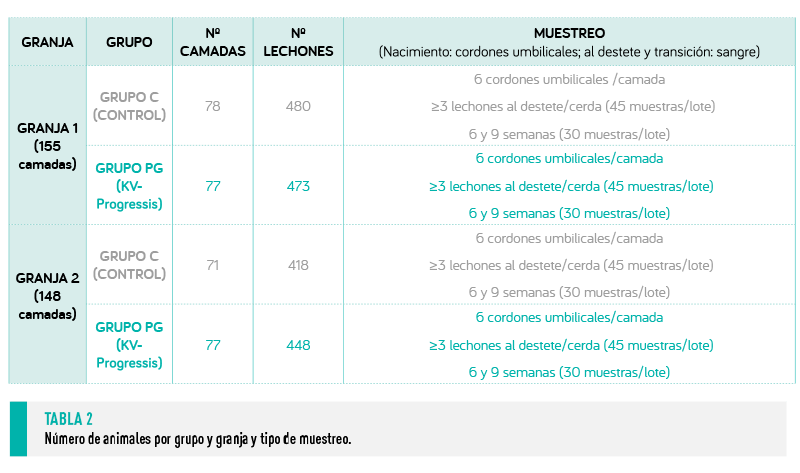
Durante seis bandas consecutivas, se establecieron dos grupos de cerdas en cada banda en función del protocolo vacunal a aplicar (Tabla 1), Grupo Control (GC) y Grupo Progressis (GP).
Los lechones descendientes de las cerdas del Grupo Progressis y del Grupo Control fueron destetados y alojados en salas de destete separadas e independientes.

En ambos grupos se seleccionan aleatoriamente lechones procedentes de diferentes camadas (Tabla 2) para evaluar los niveles de anticuerpos mediante ELISA y seroneutralización, para determinar la presencia de anticuerpos neutralizantes (AN).
RESULTADOS
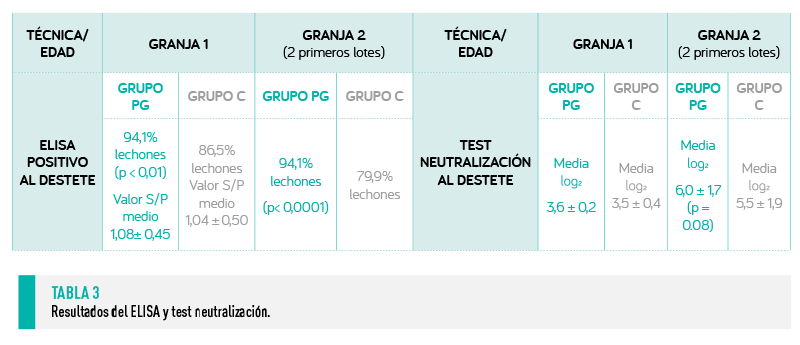
Los resultados obtenidos (Tabla 3) muestran una mayor homogeneidad en los valores de anticuerpos de los lechones descendientes de cerdas del GP, presentando unos títulos de anticuerpos neutralizantes más elevados, con una mayor proporción de animales ELISA positivos, lo que sugiere que este protocolo potencia la inmunidad humoral neutralizante frente al virus.
En este trabajo no se observaron diferencias en la productividad al parto o en el número de camadas positivas a PRRSv al nacimiento. Sin embargo, los valores obtenidos de Ct >30 (Tabla 4) muy probablemente pueden estar relacionados con una contaminación ambiental de las instalaciones, secreciones de cerdas o lechones de la camada infectados.
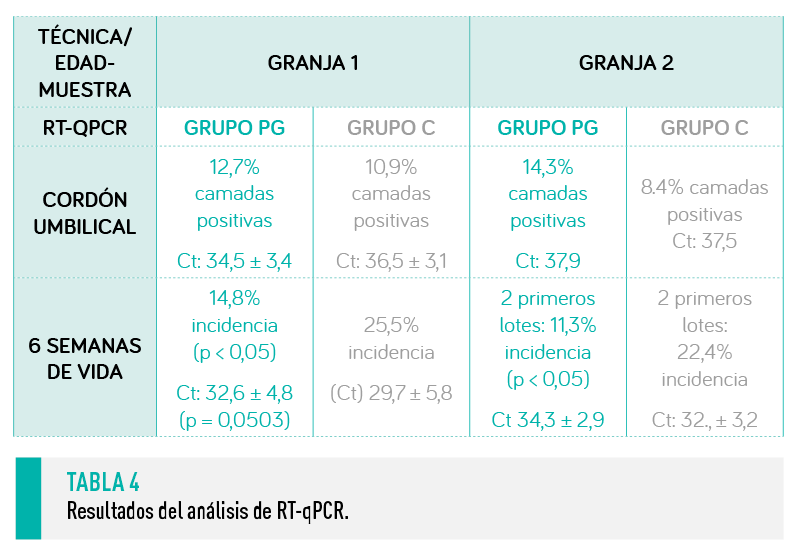
En la mayoría de los lotes, la incidencia de PRRSv a las 4 o 6 semanas de vida fue menor en los lechones del GP, lo que puede estar relacionado con una mayor proporción de animales seropositivos al destete, sugiriendo un efecto beneficioso de la vacunación preparto.
|
ESTOS RESULTADOS REFLEJAN EL IMPACTO DE LA VACUNACIÓN CON UNA SOLA DOSIS DE VACUNA INACTIVADA ANTES DEL PARTO, CON LO QUE CABRÍA DEDUCIR QUE, A TRAVÉS DE SUCESIVAS VACUNACIONES EN LOS SIGUIENTES CICLOS, SE LOGRARÍAN AUMENTAR LAS DIFERENCIAS OBSERVADAS

EXPERIENCIA DE CAMPO Nº 2
ERRADICACIÓN DE PRRSV
DISEÑO EXPERIMENTAL
Esta experiencia se realizó en una granja de ciclo cerrado de Hungría con 1.250 reproductoras y 225 cerdas de reposición (auto-reposición) infectada por PRRSv en 2008.
Al mes de la infección, se inició un protocolo de inmunización frente a PRRS que se mantuvo hasta 2014 y que incluyó la aplicación de una vacuna inactivada (Progressis®, Ceva).
A partir de ese momento, comenzó un programa nacional de erradicación del virus, con lo que se intensificó el desecho de cerdas, produciéndose lechones de 70-80 días de vida, además de continuar con la producción cerdas de reposición.
Las cerdas de reposición se vacunaban con 5 dosis de vacuna inactivada:
LA VACUNACIÓN SOSTENIDA EN EL TIEMPO CON ESTE PROTOCOLO PERMITE PRODUCIR ANIMALES NEGATIVOS A PRRSV MEDIANTE LA TÉCNICA RT-PCR A LOS 90 DÍAS DE VIDA
En una siguiente fase, las cerdas de reposición se transportaban desde la granja de reproductoras (Granja A) a dos naves vacías (Granjas B y C) que estaban alejadas 6-20 km de la granja A y de otras granjas endémicas a PRRSv.
| Las cerditas de reposición producidas en la Granja A se llevaban negativas a PRRSv (RT-PCR) con 7 semanas de vida a la Granja B, permaneciendo allí hasta las 14 semanas de vida, y siendo trasladadas posteriormente a la Granja C tras confirmar que eran serológicamente negativas a PRRSv. |  |

| Al mismo tiempo, en la Granja A se dejó de inseminar y todas las cerdas fueron sacrificadas después del último parto, realizándose una limpieza y desinfección de esta granja y, aproximadamente, a los 3 meses una repoblación con nulíparas gestantes libres de PRRSv, procedentes de la Granja C. |
RESULTADOS
| La clasificación de la Granja A como libre de PRRSv se estableció testando serológicamente a todas las cerdas dos veces con un intervalo de seis meses y fue declarada libre de PRRSv en 2019, manteniendo ese estado libre del virus (17 de febrero de 2022). |

CONCLUSIONES
De los trabajos expuestos en este artículo se puede concluir lo siguiente:
Este objetivo está apoyado en protocolos de vacunación que incluyen una vacuna inactivada.

2 La combinación de estrictas medidas de bioseguridad y manejo (realizar la fase de engorde fuera de la granja de reproductoras, aumento del desecho de cerdas, adecuada gestión de la reposición, etc.), junto a la realización de una vacunación regular con una vacuna inactivada puede proporcionar animales negativos a PRRSv y ha demostrado ser clave en el éxito de un programa de erradicación de PRRS.
BIBLIOGRAFÍA
Berton P, Normand V, Martineau GP, Bouchet F, Lebret A, WaretSzkuta A. Evaluation of porcine reproductive and respiratory syndrome stabilization protocols in 23 French Farrow-to-finish farms located in a high-density swine area. Porcine Health Manag. 2017;3:11.
Boivent et al, 2016. 24th IPVS/8th ESPHM
Defoort et al, 2014. Proceedings 23rd IPVS, p:565
Dekens et al, 2013. Proceedings 5th ESPHM, p: 190
Díaz I, Gimeno M, Callén A, Pujols J, López S, Charreyre C, et al. Comparison of different vaccination schedules for sustaining the immune response against porcine reproductive and respiratory syndrome virus. Vet J. 2013;197:438–44.
Fablet C, Renson P, Eono F, Mahé S, Eveno E, Le Dimna M, et al. Maternally-derived antibodies (MDAs) impair piglets’ humoral and cellular immune responses to vaccination against porcine reproductive and respiratory syndrome (PRRS). Vet Microbiol. 2016;192:175–80
Holtkamp DJ, Kliebenstein JB, Neumann EJ, Zimmerman JJ, Rotto HF, Yoder TK, et al. Assessment of the economic impact of porcine reproductive and respiratory syndrome virus on United States pork producers. J Swine Health Prod. 2013;21:72–84
Jung-Ah L, Nak-Hyung L, Joong-Bok L, Seung-Yong P, Chang-Seon S, In-Soo C, et al. Augmented immune responses in pigs immunized with an inactivated porcine reproductive and respiratory syndrome virus containing the deglycosylated glycoprotein 5 under feld conditions. Clin Exp Vaccine Res. 2016;5:70–4.
Knockaert et al, 2015. 7th ESPHM
Lopez OJ, Oliveira MF, Garcia EA, Kwon BJ, Doster A, Osorio FA. Protection against porcine reproductive and respiratory syndrome virus (PRRSV) infection through passive transfer of PRRSV-neutralizing antibodies is dose dependent. Clin Vaccine Immunol. 2007;14:269–75
Martín-Valls GE, Mortensen P, Clilvert H, Li Y, Cortey M, Sno M,Barna T, Terré M, Guerra N, Mareu E. The use of a whole inactivated PRRS virus vaccine administered in sows and impact on maternally derived immunity and timing of PRRS virus infection in piglets. Vet Rec Open. 2022;9:e34
Martín-Valls GE, Hidalgo M, Cano E, Mateu E. Testing of umbilical cords by real time PCR is suitable for assessing vertical transmission of porcine reproductive and respiratory syndrome virus under field conditions. Vet J. 2018;4:27–9
Nilubol et al, 2007. 5th ISERPD, p:146 Pertich A, Barna Z, Makai O, Farkas J, Molnár T, Bálin A, Szabó I, Albert M. Elimination of porcine reproductive and respiratory syndrome virus infection using an inactivated vaccine in combination with a roll-over method in a Hungarian large-scale pig herd. Acta Veterinaria Scandinavica. 2022; 64:12
Schindler et al, 2019. Proceedings 11th ESPHM, IMMPP- 46, p:312
Schindler et al, 2019. Proceedings 11th ESPHM, VVDPP-52, p:417
Spaans et al, 2016. 24th IPVS/8th ESPHM
Willems et al, 2015. Proceedings 7th ESPHM p:165
Yoon IJ, Joo HS, Goyal SM, Molitor TW. A modified serum neutralization test for the detection of antibody to porcine reproductive and respiratory syndrome virus in swine sera. J Vet Diagn Invest. 1994;6: 289–92.
Zimmerman et al, 2012. 10th edition Diseases of Swine
