Detección rápida de bacterias resistentes tras el tratamiento con enrofloxacina
Para leer más contenidos de Revista porciSapiens Abril 2023
Para leer más contenidos de Revista porciSapiens Abril 2023
| La aparición de antibiorresistencias entre los microorganismos, tanto patógenos como comensales, es un problema que genera una creciente preocupación en todo el mundo, ya que este fenómeno es responsable de la pérdida de eficacia de los antibióticos frente a enfermedades infecciosas que habitualmente tenían cura.
Es por ello que llevar a cabo un control adecuado de la existencia de estos microorganismos, conociendo cuáles son e incluso qué sensibilidad presentan frente a los antibióticos, resulta de gran importancia de cara a frenar su expansión y gestionar de una forma más eficiente los eventuales brotes que puedan producirse en las explotaciones porcinas. |
La creciente preocupación sobre la generación de resistencias antibióticas existente en la actualidad, junto con las pautas de la Agencia Europea del Medicamento hacia una reducción en la administración de antibióticos, una mejor selección de la terapia antibiótica efectiva mediante la realización de antibiogramas y la categorización de los antibióticos para su administración en medicina humana/veterinaria (EMA, 2020), han sido responsables de una reducción ostensible de su consumo en ganadería (EFSA, 2021). Sin embargo, las antibiorresistencias todavía son responsables de un elevado número de decesos anualmente (O´Neill, 2014; Wall et al., 2016; WHO, 2019; WHO, 2021).
Teniendo en cuenta que la administración de antibióticos en producción animal es en muchos casos necesaria para mantener un adecuado estatus sanitario y un buen nivel productivo, encontrar un equilibrio entre ambos aspectos puede resultar difícil.
| Un conocimiento más profundo de los efectos que los tratamientos terapéuticos con antibióticos tienen sobre poblaciones bacterianas, como la microbiota intestinal y genital de individuos tratados, podría resultar de gran ayuda en el momento de tomar la decisión de seleccionar el tratamiento más adecuado y gestionar de forma más eficiente las implicaciones posteriores del mismo. |

Entre estas bacterias, los enterococos resistentes a la vancomicina (VRE) y las enterobacterias productoras de betalactamasas de espectro extendido (ESBL) son consideradas una amenaza para la salud pública (Fournier et al., 2012; Adler et al., 2016; Madec et al., 2017; EFSA, 2021).
Los enterococos forman parte de la microbiota de animales y humanos, siendo bacterias ubicuas que se pueden encontrar en agua, suelos y plantas (Novais et al., 2013), pudiendo diseminarse a través de heces, alimentos contaminados o por contacto directo con animales (Novais et al., 2013; Nilsson et al., 2012).

Puesto que la vancomicina es uno de los antibióticos de elección para el tratamiento de infecciones causadas por enterococos multirresistentes en medicina humana, la presencia de VRE en animales es especialmente preocupante (Hammerum, 2012) y su uso en Medicina Veterinaria está prohibido de acuerdo a la categorización de la EMA (EMA, 2020).
Las enterobacterias forman parte de la microbiota habitual del tracto gastrointestinal de animales y humanos, y uno de sus principales mecanismos de resistencia es a través de la producción de β-lactamasas (Doi et al., 2017).
Es por ello que los ESBL son de especial importancia, ya que son capaces de contrarrestar el efecto de la mayor parte de los β-lactámicos, a excepción de los carbapenems y cefamicinas (Tamta et al., 2020).
Los ESBL se han encontrado frecuentemente en animales de granja, entre ellos el porcino (Stefani et al., 2014), desde donde pueden pasar a humanos.

Puesto que el grado de resistencias a antibióticos detectado en animales de producción se ha relacionado con la administración de antibióticos, se puede hablar de la existencia de [registrados]una presión positiva hacia la selección de bacterias resistentes (Tan et al., 2018; Aasmäe et al., 2019).
La enrofloxacina es una fluoroquinolona utilizada para el tratamiento de un amplio rango de enfermedades en Medicina Veterinaria, pasando por infecciones respiratorias y gastrointestinales en cerdos (De Smet et al., 2020) y, puesto que podría afectar de forma directa a la microbiota comensal, podría ser responsable de la selección de bacterias resistentes (De Smet et al., 2020).
| Es por ello que el objetivo de este trabajo fue evaluar el impacto del tratamiento con enrofloxacina vía intramuscular en cerdos sobre la aparición de VRE y ESBL en mucosa genital y rectal. |
NUEVOS AVANCES EN IDENTIFICACIÓN MICROBIANA
Actualmente, existe una gran variedad de métodos para la identificación microbiana, desde las tradicionales galerías de identificación bioquímica hasta los más novedosos métodos de identificación cromatográfica.
Entre este abanico de métodos, los sistemas automatizados de identificación microbiana*, destacan por su versatilidad y la posibilidad de llevar a cabo no solo la identificación sino también el estudio de la susceptibilidad antibiótica de un amplio abanico de microorganismos de una forma precisa, barata y rápida.
*Vitek®2 Compact (BioMérieux, Marcy-l’Étoile, Lyon, Francia)
La rapidez en el diagnóstico del agente causal de una infección no solo reduce la morbilidad y mortalidad, sino que puede ser clave a la hora de frenar la propagación de la infección.

Tanto para llevar a cabo la identificación como la evaluación de la sensibilidad antibiótica, estos equipos realizan diversas pruebas bioquímicas reunidas en tarjetas de identificación que se inoculan de forma sencilla y estandarizada con un cultivo procedente de la muestra a identificar.
LAS TARJETAS DE IDENTIFICACIÓN SON ECONÓMICAS, FÁCILES DE USAR Y GENERAN POCOS RESIDUOS EN COMPARACIÓN CON OTROS MÉTODOS, ADEMÁS DE MINIMIZAR SITUACIONES DE CONTAMINACIÓN CRUZADA CON AEROSOLES, SALPICADURAS, VERTIDOS O CONTACTO

| Una vez obtenidos los resultados, el equipo conecta de forma automática con las bases de datos que tiene asociadas para dar el resultado requerido, que se recibe de forma inmediata tras finalizar la identificación. Se trata de un equipo automatizado, eficiente e innovador, de fácil manejo y de gran utilidad en su campo, ya que, además de todas estas características, mejora el flujo de trabajo al reducir los tiempos de espera para la identificación microbiana o la evaluación de la resistencia antibiótica de los microorganismos deseados. |
Puesto que es capaz de identificar una amplia gama de microorganismos (bacterias gram-positivas, gram-negativas, levaduras y otros), ofreciendo un alto grado de discriminación entre especies y bajas tasas de resultados erróneos o no concluyentes, se trata de un sistema muy adecuado para su propósito. De hecho, está siento ampliamente utilizado en:



EVALUACIÓN DEL IMPACTO DE LA ENROFLOXACINA SOBRE LA MICROBIOTA PORCINA
A pesar de que son muchas las aplicaciones que los sistemas automatizados de identificación microbiana pueden tener, puesto que existe una preocupación creciente y generalizada por el incremento en las poblaciones de bacterias resistentes en animales de producción y su potencial transmisión a humanos, en el Instituto Agroalimentario de Aragón (IA2) en colaboración con la Universidad de la Rioja se planteó un estudio en el que se evaluase el impacto del tratamiento con enrofloxacina sobre la generación de resistencias, tanto en la microbiota intestinal como en la de la mucosa genital de un grupo de cerdos.
En este sentido, en muchas ocasiones, la generación de este tipo de bacterias viene ligada a la presión selectiva ejercida por los tratamientos antibióticos y conocer su impacto podría ser de gran ayuda a la hora gestionar de forma más adecuada su uso.
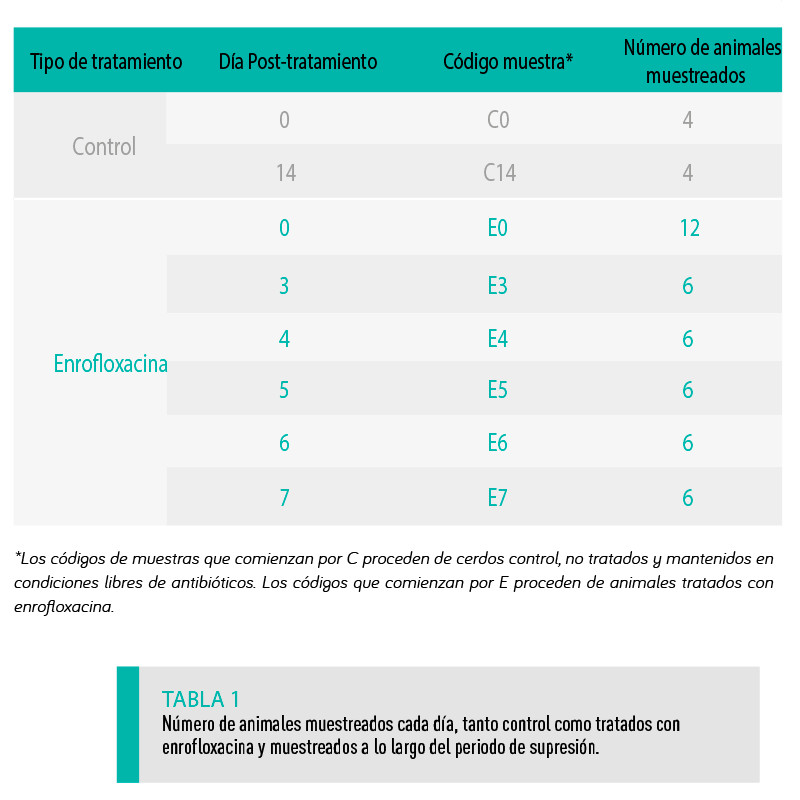
Para ello, se planteó un estudio en el que 12 cerdos recibieron una pauta completa de enrofloxacina vía intramuscular y, tras finalizar el tratamiento, se fueron tomando muestras de la mucosa rectal y genital a intervalos predeterminados dentro del periodo de supresión para llevar a cabo la identificación de microorganismos comúnmente utilizados en el estudio del efecto de los tratamientos antibióticos sobre la generación de antibiorresistencias en producción porcina:
EL ESTUDIO PERMITIÓ PERFILAR LA IMPLICACIÓN DEL TRATAMIENTO INTRAMUSCULAR CON ENROFLOXACINA EN LA SELECCIÓN DE VRE Y ESBL
DISEÑO EXPERIMENTAL

Una vez finalizado el tratamiento, se tomaron muestras de la mucosa genital y del recto, utilizando un hisopo estéril, a lo largo de todo el periodo de supresión.

La Tabla 1 muestra los días en los que se tomaron muestras tras la finalización del tratamiento.
AISLAMIENTO E IDENTIFICACIÓN BACTERIANA
De cara al aislamiento bacteriano, se utilizaron CHROMID® VRE y CHROMID® ESBL (BioMérieux, Marcy l’Etoile, France), que se sembraron e incubaron a 37°C durante 24h en condiciones de aerobiosis para la selección de E. faecium y E. faecalis resistentes a vancomicina y enterobacterias productoras de ß-lactamasas, respectivamente.
Las colonias sospechosas se confirmaron mediante el sistema automatizado de identificación microbiana. Todos estos métodos son fiables para la identificación de E. faecalis, E. faecium, E. coli y K. pneumoniae (Fang et al., 2012; Bilecen et al., 2015).
PARA CALCULAR EL PORCENTAJE DE ANIMALES CON MICROBIOTA RESISTENTE, SE CONSIDERARON POSITIVOS LOS ANIMALES QUE ALBERGABAN AL MENOS UN TIPO DE MICROORGANISMO RESISTENTE
RESULTADOS
ENTEROCOCOS RESISTENTES A LA VANCOMICINA (VRE )
![]()
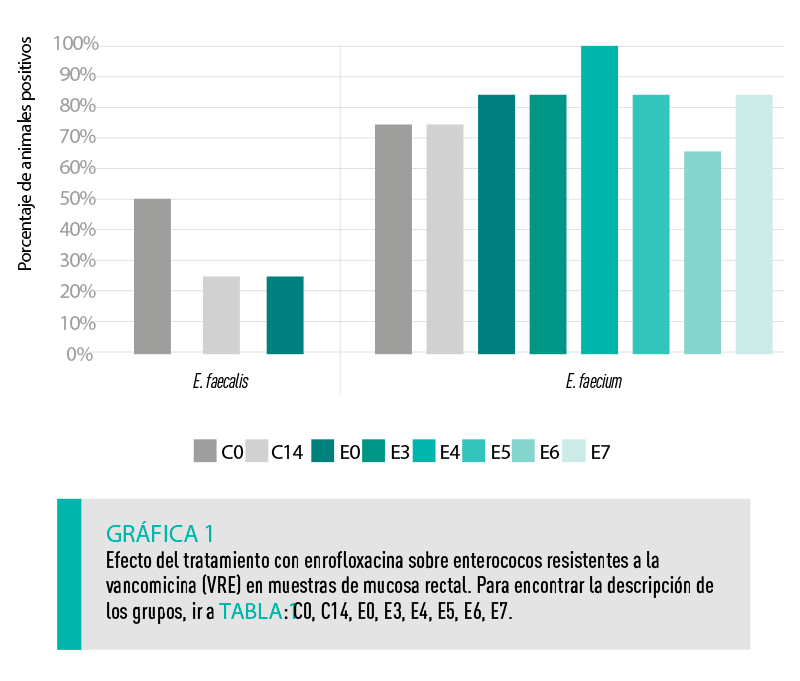
La Gráfica 1 muestra el porcentaje de animales con aislados VRE en muestras de mucosa rectal.
| GRUPO CONTROL En el grupo control, que no recibió ningún tratamiento antibiótico y se crio en condiciones libres de antibióticos, se detectó E. faecium en el 75% de los animales en los días 0 y 14, y E. faecalis en el 50% y 25%, respectivamente (C0, C14). |
GRUPO EXPERIMENTAL En los cerdos tratados con enrofloxacina, E. faecium resistente a la vancomicina (VRE) se detectó en el 83% de los animales en los días 0 y 7 y en el 100% en el día 4, mientras que E. faecalis se detectó únicamente en el 25% de los animales en el día 0. |
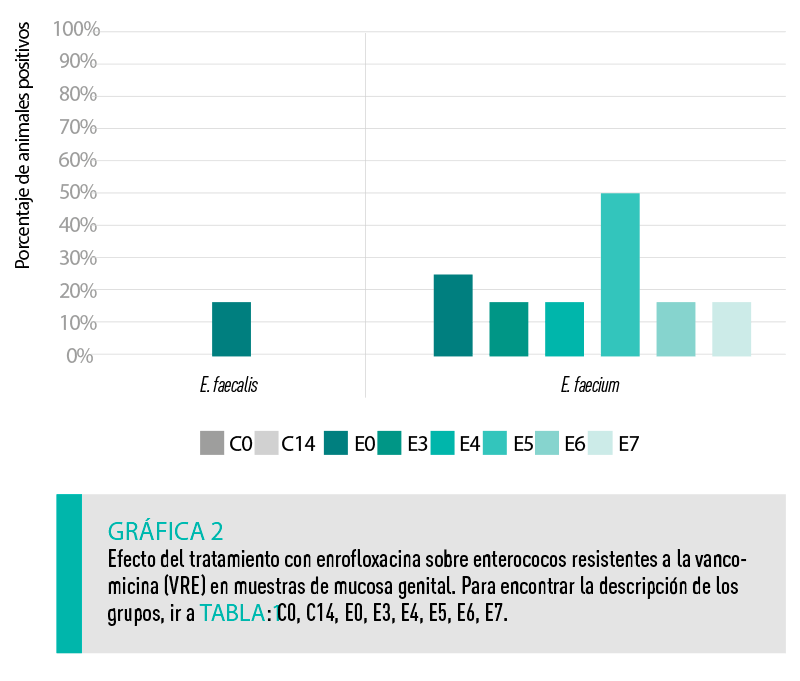
La Gráfica 2 muestra el porcentaje de animales en los que se detectaron VRE en muestras de mucosa genital de animales tratados intramuscularmente con enrofloxacina.

POBLACIONES PRODUCTORAS DE BETALACTAMASAS DE ESPECTRO EXTENDIDO (ESBL)
![]()
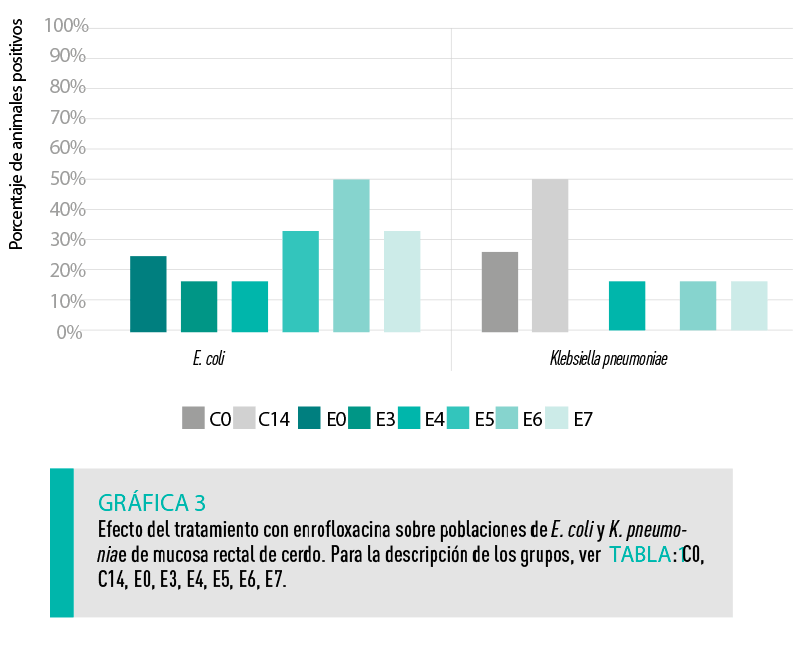
La Gráfica 3 muestra el porcentaje de animales en que se detectaron E. coli y K. pneumoniae productoras de ß-lactamasas (ESBL) en mucosa rectal.
| E. coli ESBL Mientras que en los animales no tratados no se detectó E. coli ESBL, sí se detectó en el 25% de los tratados en el día 0, en el 17% en los días 3 y 4 y en el 33 y 50% en los días 5 y 7, respectivamente. |
K. pneumoniae ESBL K. pneumoniae ESBL se detectó en los animales control no tratados, en los días 0 y 14, en un 25 y 50% de los animales, y en un 17% de los animales tratados en los días 4, 6 y 7, respectivamente. |
La Gráfica 4 muestra el porcentaje de animales en los que se aislaron E. coli y K. pneumoniae ESBL de mucosa genital.
| E. coli ESBL E. coli ESBL no se detectó en el grupo control, mientras que sí se encontró en el 17% y 33% de la mucosa genital de los cerdos tratados en los días 5 y 6, respectivamente. |
K. pneumoniae ESBL K. pneumoniae ESBL únicamente se detectó en mucosa genital del grupo control el día 14. |


DISCUSIÓN
Algunos estudios llevados a cabo en cerdos muestran que los aislados de Enterococcus spp. son sensibles a la vancomicina (Tan et al., 2018), mientras que otros autores han demostrado la presencia de VRE en cerdos.
Por ejemplo, Aarestrup et al. (2000) observaron que el 17% de los aislados de E. faecium en porcino de Dinamarca eran VRE.

| ENTEROCOCOS RESISTENTES A LA VANCOMICINA (VRE) En el presente estudio, se detectaron enterococos resistentes a la vancomicina, tanto en cerdos no tratados como tratados.
|
ENTEROBACTERIAS PRODUCTORAS DE BETALACTAMASAS DE ESPECTRO EXTENDIDO (ESBL) Las enterobacterias productoras de ß-lactamasas (ESBL), específicamente E. coli ESBL, son comúnmente detectadas en porcino en todo el mundo (Escudero et al., 2012; Ewers et al., 2012; Bergšpica et al., 2020; Fournier et al., 2021) en porcentajes mayores en granjas en las que se administran antibióticos de forma más frecuente (De Koster et al., 2021; Benavides et al., 2021), lo que sugiere un fenómeno de presión selectiva.
Puesto que E. coli es una bacteria típicamente intestinal, se encontraron más animales positivos en mucosa rectal en comparación con genital (Dandachi et al., 2018). Hay pocos estudios sobre K. pneumoniae ESBL, y es que sus recuentos son mucho menores en comparación con E. coli (De Koster et al., 2021).
|
LOS DATOS PRESENTADOS DEMUESTRAN LA PRESENCIA DE CEPAS RESISTENTES EN LOS ANIMALES, ESPECIALMENTE EN MUCOSA RECTAL, TRAS EL TRATAMIENTO CON ENROFLOXACINA VÍA INTRAMUSCULAR

A pesar de que la enrofloxacina se excreta principalmente por orina, también se han detectado elevadas concentraciones en heces de cerdos tras su administración intramuscular (Zhou et al., 2008) ya que también se metaboliza a nivel hepático (Giguère et al., 2013) y puede ser excretada a nivel intestinal (Álvarez et al., 2008).
Esto afecta a la microbiota intestinal, especialmente a microorganismos como E. coli, frente al que la enrofloxacina es muy efectiva (Edlund & Nord, 1999):


La microbiota de animales no tratados también podría verse afectada debido a la transferencia ambiental de estas cepas.

| La contaminación cruzada de la carne con poblaciones resistentes de origen fecal supone un importante riesgo sanitario (Wiuff et al, 2002; Ramos et al., 2012), ya que contribuye a agravar el ya preocupante fenómeno de resistencias antibióticas. |

CONCLUSIONES
Este estudio demuestra que la administración intramuscular de enrofloxacina puede seleccionar E. coli productoras de ß-lactamasas (ESBL) en el tracto intestinal y, en menor medida, a nivel genital, así como las poblaciones de E. faecium resistentes a la vancomicina (VRE), por lo que se debe tener especial cuidado para evitar la contaminación de las canales tras el sacrificio.
El sistema automatizado de identificación microbiana** ha mostrado ser un método de detección fiable, rápido y efectivo para identificar bacterias resistentes a antibióticos, aunque sus posibilidades son mucho amplias.
**El VITEK®2 utilizado en esta investigación es propiedad del Instituto Agroalimentario de Aragón IA2 – Universidad de Zaragoza y forma parte del “Servicio de Identificación y Evaluación de la Sensibilidad Antibiótica” que ofrece dentro de su cartera de servicios a entidades, empresas y centros de investigación públicos y privados.
El estudio ha sido cofinanciado al 65% por el Fondo Europeo de Desarrollo Regional (FEDER) a través del Programa Interreg V-A España-Francia- Andorra (POCTEFA 2014-2020).
Para más información, consultar la siguiente referencia: González- Fandos, E., Martínez-Laorden, A., Abad-Fau, A., Sevilla, E., Bolea, R., Serrano, M. J., … & Pagán, R. (2022). Effect of intramuscularly administered oxytetracycline or enrofloxacin on vancomycinresistant enterococci, extended spectrum beta-lactamase-and carbapenemase-producing Enterobacteriaceae in pigs. Animals, 12(5), 622.
Te puede interesar: Uso racional de antimicrobianos en porcino: antimicrobianos inhibidores de la síntesis de ARN y ADN – Parte I

REFERENCIAS
Aarestrup, F.M.; Agerso. Y.; Gerner-Smidt. P.; Madsen. M.; Jensen, L.B. Comparison of antimicrobial resistance phenotypes and resistance genes in Enterococcus faecalis and Enterococcus faecium from humans in the community, broilers, and pigs in Denmark. Diagn. Microbiol. Infect. Dis. 2000, 37, 127-137.
Aasmäe, B.; Häkkinen, L.; Kaartt, T.; Kalmus, P. Antimicrobial resistance of Escherichia coli and Enterococcus spp. isolated from Estonian cattle and swine from 2010 to 2015. Acta Vet. Scand. 2019, 61,5.
Adler, A.; Katz, D.E.; Marchaim, D. The continuing plague of extended-spectrum beta-lactamase-producing Enterobacteriaceae infections. Infect. Dis. Clin. North Am. 2016, 30, 347-375.
Álvarez A.; Pérez M.; Prieto J.; Molina A.; Real R, Merino, G. Fluoroquinolone efflux mediated by ABC transporters. J Pharm Sci. 2008, 97, 3483–3493.
Benavides, J.A.; Streicker, D.G.; Gonzales, M.S.; Rojas-Paniagua, E.; Shiva, C. Knowledge and use of antibiotics among low-income small-scale farmers of Peru. Prev. Vet. Med. 2021b, 189, 105287.
Béraud, R.; Huneault, L.; Bernier, D.; Beaudry, F.; Letellier, A.; del Castillo, J.R.E. Comparison of the selection of antimicrobial resistance in fecal Escherichia coli during enrofloxacin administration with a local drug delivery system or with intramuscular injections in a swine model. Can. J. Vet. Res., 2008, 72, 311-319.
Bergšpica, I.; Kaprou, G.; Alexa, E.A.; Prieto, M.; Alvarez-Ordóñez, A. Extended spectrum β-lactamase (ESBL) Escherichia coli in pigs and pork meat in European Union. Antibiotics 2020, 9, 678.
Bilecen, K.; Yaman, I.G.; Ciftci,U.; Laleli, Y.R. Performances and reliability of Bruker Microflex LT and VITEK MS MALDI-TOF mass spectrometry systems for the identification of clinical microorganisms BioMed Res. Int., 2015, 516410.
Cantas, L.; Suer, K.; Guler, E.; Imir, T. High emergence of ESBL producing E. coli cystitis: time to get smarter in Cyprus. Front. Microbiol. 2015, 6, 1446.
Chun, L. Y., Dolle-Molle, L., Bethel, C., Dimitroyannis, R. C., Williams, B. L., Schechet, S. A., … & Skondra, D. (2019). Rapid pathogen identification and antimicrobial susceptibility testing in in vitro endophthalmitis with matrix assisted laser desorption-ionization Time-of-Flight Mass Spectrometry and VITEK 2 without prior culture. PLoS One, 14(12), e0227071.
Dandachi, I.; Chabou, S.; Daoud, Z.; Rolain, J.M. Prevalence and emergence of extended-spectrum cephalosporin, carbapenem and colistin-resistant Gram negative bacteria of animal origin in the Mediterranean basin. Front. Microbiol. 2018, 9, 2299.
De Koster, S.; Ringenier, M.; Lammens, C.; Stegeman, A.; Tobias, T.; Velkers, F.; Vernooij, H.; Kluytmans-Van Den Bergh, M.; Kluytmans, J.; Dewulf, J.; Goossens, H. ESBL-producing, carbapenem and ciprofloxacin-resistant Escherichia coli in belgian and dutch broiler and pig farms: A cross-sectional and cross-border study. Antibiotics, 2021, 10. 945.
De Smet, J.; Boyen, F.; Croubels, S.; Rasschaert, G.; Haesebrouck, F.; Temmerman, R.; Rutjens, S.; De Backer, P.; Devreese, M. The impact of therapeutic-dose induced intestinal enrofloxacin concentrations in healthy pigs on fecal Escherichia coli populations. BMC Vet. Res. 2020, 16, 382.
Dégi, J., Cristina, R. T., Dégi, D. M., Muselin, F., Dumitrescu, C., & Iancu, I (2019). Research of methicillin resistance staphylococci in a pig’s farm. Lucrări Ştiinţifice, 27.
Doi, Y.; Iovleva, A.; Bonomo, R.A. The ecology of extended-spectrum B lactamases (ESBLs) in the developed world. J. Travel Med. 2017, 24, S44-S51.
Edlund, C.; Nord, C.E. Effect of quinolones on intestinal ecology. Drugs 1999, 58, 65-70.
EFSA, 2021. European Centre for Disease Prevention and Control (ECDC), European Food Safety Authority (EFSA), & European Medicines Agency (EMA). (2021). Third joint inter-agency report on integrated analysis of consumption of antimicrobial agents and occurrence of antimicrobial resistance in bacteria from humans and food-producing animals in the EU/EEA: JIACRA III 2016-2018. EFSA Journal, 19(6), e06712.
EMA (European Medicine Agency). Categorisation of antibiotics for use in animals for prudent and responsible use. 2020 Available online: https://www.ema.europa.eu/en/documents/report/infographic-categorisation-antibiotics-use-animals-prudent-responsible-use_en.pdf (accesed 27 April 2021)
Erwin, S.; Foster D.M.; Jacob, M.E.; Papich, M.G.; Lanzas, C. The effect of enrofloxacin on enteric Escherichia coli: Fitting a mathematical model to in vivo data. PLoS ONE 2020, 15 e0228138.
Escudero, E.; Vinue, L.; Teshager, T.; Torres, C.; Moreno, M.A. Resistance mechanisms and farm-level distribution of fecal Escherichia coli isolates resistant to extended-spectrum cephalosporins in pigs in Spain. Res. Vet. Sci. 2010, 88, 83-87.
European Food Safety Authority and European Centre for Disease Prevention and Control). The European Union Summary Report on Antimicrobial Resistance in Zoonotic and Indicator Bacteria from Humans, Animals and Food in 2018/2019. EFSA J. 2021, 19, e06490.
Ewers, C.; Bethe, A.; Semmler, T.; Guenther, S.; Wieler, L. H.. Extended spectrum beta-lactamase-producing and AmpC-producing Escherichia coli from livestock and companion animals, and their putative impact on public health: a global perspective. Clin. Microbiol. Infect. 2012, 18, 646-655.
Fang, H.; Ohlsson, A.K.; Ullberg, M.; Özenci, V. Evaluation of species-specific PCR, Bruker MS, VITEK MS and the VITEK 2 system for the identification of clinical Enterococcus isolates Eur. J. Clin. Microbiol. Infect. Dis. 2012, 31, 3073-3077.
Founou, L. L., Founou, R. C., Ntshobeni, N., Govinden, U., Bester, L. A., Chenia, H. Y., … & Essack, S. Y. (2019). Emergence and spread of extended spectrum β-lactamase producing Enterobacteriaceae (ESBL-PE) in pigs and exposed workers: a Multicentre Comparative Study between Cameroon and South Africa. Pathogens, 8(1), 10.
Fournier, C.; Nordmann, P.; Pittet, O.; Poirel, L. Does an antibiotic stewardship applied in a pig farm lead to low ESBL prevalence? Antibiotics, 2021, 10, 574.
Fournier, S.; Brun-Buisson, C.; Jarlier, V. Twenty years of antimicrobial resistance control programme in a regional multi hospital institution, with focus on emerging bacteria (VRE and CPE). Antimicrob. Resist. Infect. Control 2012, 1, 9.
Gastmeier, P.; Schröder, C.; Behnke, M.; Meyer, E.; Geffers, C. Dramatic increase in vancomycin-resistant enterococci in Germany. J. Antimicrob. Chemother. 2014, 69, 1660-1664.
Giguère S.; Prescott J.; Dowling, P. Antimicrobial therapy in veterinary medicine, 5th ed; John Wiley & Sons, New Jersey, USA, 2013.
Gundran, R. S., Cardenio, P. A., Salvador, R. T., Sison, F. B., Benigno, C. C., Kreausukon, K., … & Punyapornwithaya, V. (2020). Prevalence, Antibiogram, and Resistance Profile of Extended-Spectrum β-Lactamase-Producing Escherichia coli Isolates from Pig Farms in Luzon, Philippines. Microbial Drug Resistance, 26(2), 160-168.
Hammerum, A.M. Enterococci of animal origin and their significance for public health. Clin. Microbiol. Infect. 2012, 18, 619-625.
Hwang, I. Y., Ku, H. O., Lim, S. K., Park, C. K., Jung, G. S., Jung, S. C., & Nam, H. M. (2009). Species distribution and resistance patterns to growth promoting antimicrobials of enterococci isolated from pigs and chickens in Korea. Journal of Veterinary Diagnostic Investigation, 21(6), 858-862.
Lauderdale, T.L.; Shiau, Y.R.; Wang, H.Y.; Lai, J.F.; Huang, I.W.; Chen, P.C.; Chen, H.Y.; Lai, S.S.; Liu, Y.F.; Ho., M. Effect of banning vancomycin analogue avoparcin on vancomycin-resistant enterococci in chicken farms in Taiwan. Environ. Microbiol. 2007, 9, 819-823.
Leangapichart, T.; Lunha, K.; Jiwakanon, J.; Angkititrakul, S.; Järhult, J.D.; Magnusson, U.; Sunde, M. Characterization of Klebsiella pneumoniae complex isolates from pigs and humans in farms in Thailand: Population genomic structure, antibiotic resistance and virulence genes. J. Antimicrob. Chemoth. 2021, 76, 2012-2016.
Lim, J. S., Han, D. W., Lee, S. R., Hwang, O. H., Kwag, J. H., & Cho, S. B (2015). A Bacterial Strain Identified as Bacillus licheniformis using Vitek 2 Effectively Reduced NH 3 Emission from Swine Manure. Journal of Animal Environmental Science, 21(3), 83-92.
Liu, X.; Liu, H.; Wang, L.; Peng, Q.; Li, Y.; Zhou, H.; Li, Q. Molecular characterization of extended-spectrum β-lactamase-producing multidrug resistant Escherichia coli from swine in Northwest China. Front. Microbiol. 2018, 9, 1756
Madec, J.Y.; Haenni, M.; Nordmann, P.; Poirel, L. Extended-spectrum beta lactamase/AmpC- and carbapenemase-producing Enterobacteriaceae in animals: a threat for humans? Clin. Microbiol. Infect. 2017, 23, 826-833.
Matajira, C. E. C., Poor, A. P., Moreno, L. Z., Monteiro, M. S., Dalmutt, A. C., Gomes, V. T. M., … & Moreno, A. M. (2020). Vagococcus sp. a porcine pathogen: molecular and phenotypic characterization of strains isolated from diseased pigs in Brazil. The Journal of Infection in Developing Countries, 14(11), 1314-1319.
Mittal, D., Grakh, K., Prakash, A., Moudgil, P., Devi, B., & Jadhav, V. (2018). Isolation, Identification and Characterization of Enteric Bacteria from Post Weaning Diarrheic Pigs and their Resistance to Multiple Antibiotics. International Journal of Current and Applied Microbiology, 7, 2377-2384.
Morka, K., Bystroń, J., Bania, J., Korzeniowska- Kowal, A., Korzekwa, K., Guz Regner, K., & Bugla-Płoskońska, G. (2018). Identification of Yersinia enterocolitica isolates from humans, pigs and wild boars by MALDI TOF MS. BMC Microbiology, 18(1), 1-10.
Nilsson, O. Vancomycin resistant enterococci in farm animals. Occurrence and importance. Infect. Ecology Epidemiol. 2012, 2, 16959.
Novais, C.; Freitas, A.R.; Silveira, E.; Antunes, P.; Silva, R.; Coque, T.M.; Peixe, L. Spread of multidrug-resistant Enterococcus to animals and humans: an underestimated role for the pig farm environment. J. Antimicrob. Chemother. 2013, 68, 2746-2754.
O’Neill, J. Antimicrobial Resistance: Tackling a Crisis for the Health and Wealth of Nations. London: Review on Antimicrobial Resistance; 2014. Available online: https://amr-review.org/sites/default/files/AMR%20Review%20Paper%20.%20Tacklng%20a%20crisis%20for%20the%20health%20and%20wealth%20of%20nations_1.pdf (accessed on 2 November 2021).
Ojer-Usoz, E.; Gonzalez, D.; Vitas, A.I.; Leiva, J.; Garcia-Jalon, I.; Febles Casquero, A.; Escolano, M.S. Prevalence of extended-spectrum beta lactamase-producing Enterobacteriaceae in meat products sold in Navarra, Spain. Meat Sci. 2013, 93, 316-321.
Picozzi, S.C.M.; Casellato, S.; Rossini, M.; Paola, G.; Tejada, M.; Costa, E.; Carmignani L. Extended-spectrum beta-lactamase-positive Escherichia coli causing complicated upper urinary tract infection: Urologist should act in time. Urol. Annals. 2014, 6, 107-112.
Ramos, S.; Igrejas, G.; Capelo-Martinez, J.L.; Poeta, P. Antibiotic resistance and mechanisms implicated in fecal enterococci recovered from pigs, cattle and sheep in a Portuguese slaughterhouse. Ann. Microbiol. 2012, 62, 1485-1494.
Stefani, S.; Giovanelli, I.; Anacarso, I.; Condo, C.; Messi, P.; de Niederhausern, S.; Bondi, M.; Iseppi, R.; Sabia, C. Prevalence and characterization of extended-spectrum beta-lactamase- producing Enterobacteriaceae in food producing animals in Northern Italy. New Microbiol. 2014, 37, 551-555.
Taipa, R., Lopes, V., & Magalhães, M. (2008). Streptococcus suis meningitis: first case report from Portugal. Journal of Infection, 56(6), 482-483.
Tamta, S.; Vonodh-Kumar, O.R.; Pruthvishree, B.S.; Karthikeyan, R.; Ramkumar, R.R.; Chethan, G.E.; Dubal, Z.B.; Sinha, D.K.; Singh, B.R. Faecal carriage of extended spectrum beta-lactamase (ESBL) and New Delhi metallobeta-lactamase(NDM) producing Escherichia coli between piglets and pig farmworkers. Comparative Immunol. Microbiol. Infect. Dis. 2020, 73, 101564.
Tan, S.C.; Chong, C.W.; Teh, C.S.J.; Ooi, P.T.; Thong, K.L. Occurrence of virulent multidrug resistant Enterococcus faecalis and Enterococcus faecium in the pigs, farmers and farm environments in Malaysia. Peer J. 2018, 6, e5353.
Unal, N.; Bal, E.; Kapagoz, A.; ALtun, B.; Kozag, N. Detection of vancomycin resistant enterococci in samples from broiler flocks and houses. Acta Vet. Hungarica 2020, 68,117-122.
Wall, B.A.; Mateus, A.; Marshall, L.; Pfeiffer, D.; Lubroth, J.; Ormel, H.J.; Otto, P.; Patriarchi, A. Food and Agriculture Organization of the United Nations. Drivers, dynamics and epidemiology of antimicrobial resistance in animal production. Food and Agriculture Organization (FAO): Rome, Italy, 2016.
Wist, V.; Morach, M.; Schneeberger, M.; Cernela, N.; Stevens, M.J.A.; Zurfluh, K.; Stephan, R.; Nüesch-Inderbinen, M. Phenotypic and genotypic traits of vancomycin-resistant enterococci from healthy food-producing animals. Microorganisms 2020, 8, 261.
Wiuff, C.; Lykkesfeldt, J.; Aarestrup, F.M.; Svendsen, O. Distribution of enrofloxacin in intestinal tissue and contents of healthy pigs after oral and intramuscular administrations. J. Vet. Pharmacol. Therap. 2002, 25, 335-342.
World Health Organization. Antibacterial agents in clinical development: an analysis of the antibacterial clinical development pipeline; World Health Organization, Geneva, Switzerland, 2019. Available online: http://www.who.int (accessed on 18 Nov 2021).
World Health Organization. Global Antimicrobial Resistance and Use Surveillance System (GLASS) Report. World Health Organization, Geneva, Switzerland, 2021. Available online: http://www.who.int (accessed on 18 Nov 2021).
Zhou, X.J.; Chen, C.X.; Yue, L.; Sun Y.X.; Ding, H.Z.; Liu, Y.H. Excretion of enrofloxacin in pigs and its effect on ecological environment. Environ. Toxicol. Phar. 2008, 26, 272–277.
[/registrados]
