La Peste Porcina Africana (PPA), la mayor amenaza para el sector porcino de todo el mundo, se ha propagado a más de 55 países en tres continentes, estimándose una afectación de más del 77% de la población porcina mundial.
Desarrollar una vacuna frente al VPPA que sea aplicable en jabalíes silvestres nos llevará un paso más cerca de evitar su transmisión a cerdos domésticos.

La Peste Porcina Africana (PPA), la mayor amenaza para el sector porcino de todo el mundo, se ha propagado a más de 55 países en tres continentes, estimándose una afectación de más del 77% de la población porcina mundial.
En la UE, el jabalí silvestre (Sus scrofa) es el hospedador más importante. De hecho, los principales factores que han facilitado la propagación constante y sin precedentes de la PPA por Europa son:
![]() El comercio
El comercio
![]() El movimiento continuado de las poblaciones de jabalíes infectados entre las distintas regiones
El movimiento continuado de las poblaciones de jabalíes infectados entre las distintas regiones
![]() La ausencia de una vacuna para prevenir la infección
La ausencia de una vacuna para prevenir la infección
LA PPA PERFILA EL NUEVO ORDEN MUNDIAL PORCINO
La Peste Porcina Africana es una de las enfermedades víricas de mayor impacto en el sector porcino, ya que las cepas virulentas del virus provocan fiebre hemorrágica aguda o hiperaguda en los animales con una mortalidad de hasta el 100%.
Debido a sus devastadoras consecuencias socioeconómicas y sobre la salud animal, la PPA está catalogada como una Enfermedad de Declaración Obligatoria a la OIE.
 A falta de una vacuna o un tratamiento específico eficaz frente a la PPA[registrados], el control de la enfermedad se basa en la despoblación y las restricciones en el comercio local, nacional e internacional de los cerdos vivos y sus productos derivados.
A falta de una vacuna o un tratamiento específico eficaz frente a la PPA[registrados], el control de la enfermedad se basa en la despoblación y las restricciones en el comercio local, nacional e internacional de los cerdos vivos y sus productos derivados.
EPIDEMIOLOGÍA DE LA PPA
Tras su introducción en Georgia desde el Este de África, el genotipo II del virus de la PPA (VPPA) ha estado circulando por el Este de Europa desde el 2007, por la UE desde el 2014 y por Asia desde el 2018.
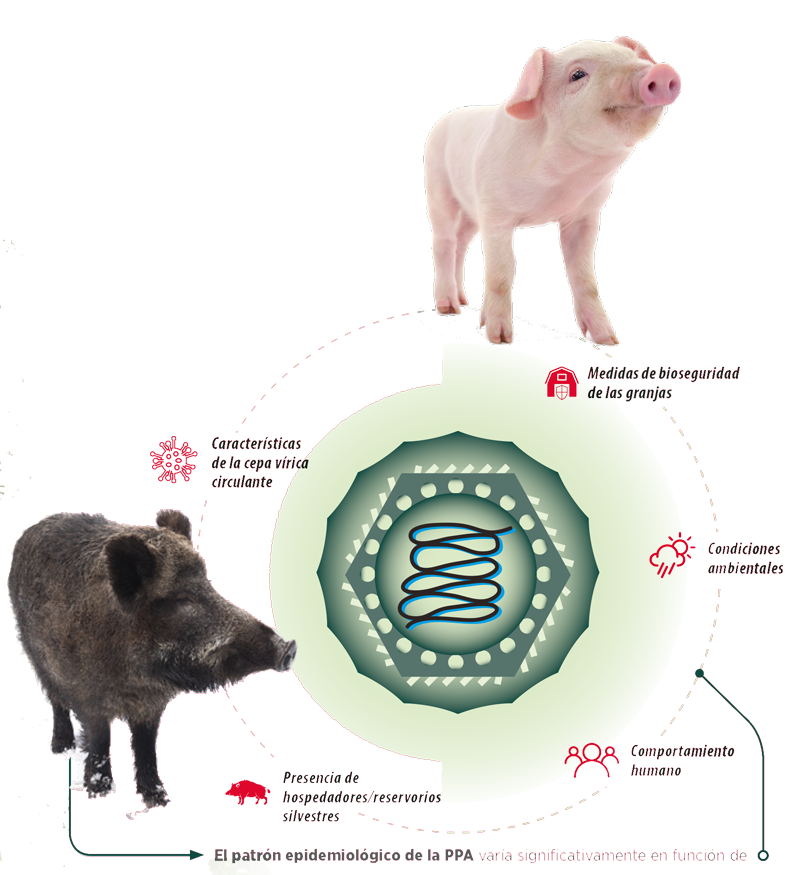
En los últimos 5 años, 11 países de la UE (Lituania, Polonia, Letonia, Estonia, República Checa, Hungría, Bulgaria, Bélgica Rumanía, Eslovaquia e Italia) han notificado casos de PPA, pudiendo atribuirse el 90% de los casos al jabalí. Por ello, un análisis epidemiológico llevado a cabo en Estonia concluyó que el jabalí silvestre es el principal factor de riesgo para la transmisión de la PPA en Europa.
El mantenimiento y la propagación del virus, que se mantiene de forma endémica en las poblaciones de jabalíes silvestres de la UE, se ha visto facilitada por el movimiento de los animales infectados por el territorio europeo.

CLÍNICA DE LA PPA
Las manifestaciones clínicas de la PPA dependen de varios factores, como la virulencia de la cepa, el hospedador, la dosis infectante y la vía de infección.
Con un periodo de incubación de 3-19 días, la enfermedad se manifiesta con:
![]() Signos clínicos y lesiones congestivas: hemorragia, edema, ascitis y shock
Signos clínicos y lesiones congestivas: hemorragia, edema, ascitis y shock
![]() Afectación de los sistemas digestivo y respiratorio
Afectación de los sistemas digestivo y respiratorio
![]() Mortalidad del 10-100% (dependiendo de la virulencia de la cepa)
Mortalidad del 10-100% (dependiendo de la virulencia de la cepa)
Si bien, los estudios recientes señalan la circulación de cepas moderadamente virulentas de VPPA, las cepas del genotipo II responsables de los brotes eurasiáticos son altamente virulentas, induciendo una forma clínica aguda con una mortalidad de casi el 100% en cerdos domésticos y jabalíes silvestres.
CON LA MIRADA PUESTA EN LA VACUNACIÓN
Contar con una vacuna eficaz frente a la PPA se ha convertido en una prioridad para el sector porcino global y, sin embargo, se ha visto obstaculizada por:
![]() La complejidad genética del VPPA.
La complejidad genética del VPPA.
![]() La falta de conocimientos sobre la inmunidad frente al virus.
La falta de conocimientos sobre la inmunidad frente al virus.
![]() La falta de desarrollo de anticuerpos neutralizantes.
La falta de desarrollo de anticuerpos neutralizantes.
![]() Dificultades técnicas, como la falta de líneas celulares estables.
Dificultades técnicas, como la falta de líneas celulares estables.
En Europa, el interés por desarrollar una vacuna efectiva ha ido en aumento:
![]() La vacunación con virus inactivados o vacunas de subunidades no ha logrado inducir una buena inmunidad protectora.
La vacunación con virus inactivados o vacunas de subunidades no ha logrado inducir una buena inmunidad protectora.
![]() Las vacunas vivas atenuadas obtenidas mediante pases seriados en cultivos celulares o mediante deleciones genéticas pueden inducir una protección parcial o completa.
Las vacunas vivas atenuadas obtenidas mediante pases seriados en cultivos celulares o mediante deleciones genéticas pueden inducir una protección parcial o completa.
El diseño de candidatos vacunales atenuados se ha visto facilitado por la identificación de los genes del VPPA relacionados con la virulencia y la evasión de la respuesta inmunitaria.
Por otro lado, también ha sido posible aislar candidatos vacunales atenuados de forma natural en el campo. Un ejemplo es la cepa del VPPA poco virulenta y no hemadsorbente aislada a partir de un jabalí silvestre cazado en Letonia en 2017 (Lv17/WB/Rie1).
 La infección experimental de cerdos domésticos con esta cepa ha logrado proporcionar protección frente a una cepa altamente virulenta, hemadsorbente, del genotipo II del VPPA (Arm07), lo que sugiere que podría usarse la cepa Lv17/WB/Rie1 como vacuna viva atenuada.
La infección experimental de cerdos domésticos con esta cepa ha logrado proporcionar protección frente a una cepa altamente virulenta, hemadsorbente, del genotipo II del VPPA (Arm07), lo que sugiere que podría usarse la cepa Lv17/WB/Rie1 como vacuna viva atenuada.
¿EL CONTROL DE LA PPA PODRÍA PASAR POR LA VACUNACIÓN DE LOS JABALÍES?
Existe un enorme interés en desarrollar una vacuna frente a VPPA que sea aplicable en jabalíes silvestres. Ya la vacunación de estos animales demostró ser una herramienta muy valiosa para el control de la Peste Porcina Clásica (PPC). Sin embargo, hasta ahora solo se han realizado ensayos en cerdos domésticos.
 Por ello, en este estudio, se demuestra que la inmunización oral de jabalíes con el virus atenuado Lv17/WB/Rie1 confiere una protección del 92% al desafiar a los animales por una cepa virulenta del VPPA (Arm07).
Por ello, en este estudio, se demuestra que la inmunización oral de jabalíes con el virus atenuado Lv17/WB/Rie1 confiere una protección del 92% al desafiar a los animales por una cepa virulenta del VPPA (Arm07).
DISEÑO EXPERIMENTAL
![]() JABALÍ
JABALÍ
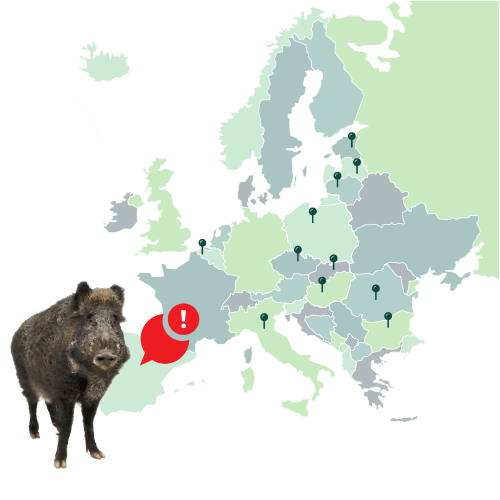
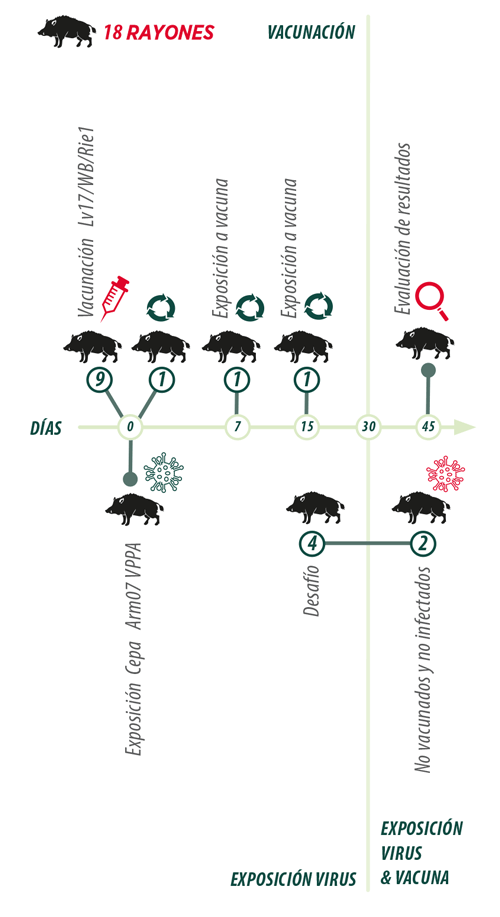
El estudio se realizó con 18 rayones de 3-4 meses y 10-15 kg procedentes de una granja de jabalíes de Extremadura alojadas en las instalaciones de Biocontención BSL-3 de VISAVET y con alimentación ad libitum.
VACUNA PPA
Para la inmunización de los animales se empleó el genotipo II no hemadsorbente del VPPA (Lv17/WB/Rie1).
![]() Este virus no hemadsorbente cuenta con una mutación en el gen EP402R que da lugar a una proteína truncada.
Este virus no hemadsorbente cuenta con una mutación en el gen EP402R que da lugar a una proteína truncada.
![]() Para el desafío de los animales se utilizó la cepa hemadsorbente Arm07 del genotipo II del VPPA.
Para el desafío de los animales se utilizó la cepa hemadsorbente Arm07 del genotipo II del VPPA.
 VACUNACIÓN ORAL
VACUNACIÓN ORAL
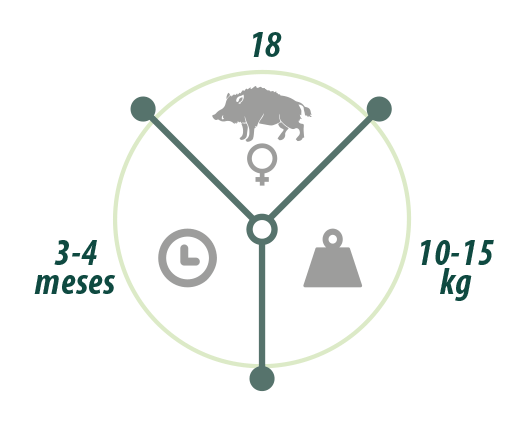
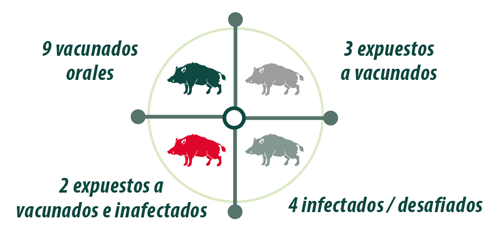
Durante el experimento, 12 de los 18 rayones participaron en el ensayo de vacunación que duró 30 días para poder valorar el desarrollo de una respuesta inmunitaria protectora y la transmisión de la vacuna a otros animales por contacto:
Para valorar la eficacia protectora de la vacuna frente a una cepa virulenta del VPPA, se expusieron los rayones vacunados a 4 rayones que habían sido inoculados por vía intramuscular con 10 HAD50** de la cepa Arm07 del VPPA.
* TCID50: Cantidad de virus que provocan efectos citopáticos en el 50% de los medios de cultivo infectados ( TCID50/ml).
**HAD50: Cantidad de virus que provocan hemadsorción en el 50% de los medios de cultivo infectados (HAD50/ml/TCID50/ml).
 DESAFÍO
DESAFÍO
Además, 30 días después de la vacunación, 2 rayones no vacunados y no infectados fueron expuestas a todos los animales para determinar la transmisión de la vacuna o de la cepa virulenta.
 EVALUACIÓN
EVALUACIÓN
A lo largo de todo el ensayo, se monitorizaron los siguientes parámetros:
Al finalizar el periodo de estudio (54 días tras la vacunación) se realizó un examen postmortem de los animales para evaluar la presencia de lesiones macroscópicas compatibles con PPA y para la detección del VPPA en los tejidos analizados (médula ósea, cerebro, linfonodos gastrohepáticos, corazón, riñón, pulmón, nódulos linfáticos, bazo y vejiga).
EFICACIA DE LA VACUNACIÓN ORAL FRENTE A LA PPA EN JABALÍES 
 NIVEL DE ANTICUERPOS
NIVEL DE ANTICUERPOS
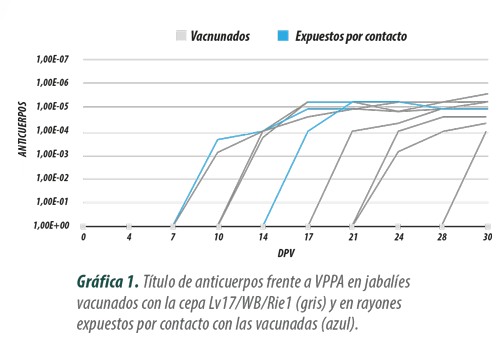
El análisis de los resultados del ensayo demuestra que la cepa Lv17/ WB/Rie1, administrada oralmente, es capaz de inducir la producción de anticuerpos en los jabalíes silvestres (Gráfica 1).
![]() Durante el periodo de vacunación, 6 de las 9 rayones vacunados por vía oral produjeron anticuerpos a partir del día 15 postvacunación.
Durante el periodo de vacunación, 6 de las 9 rayones vacunados por vía oral produjeron anticuerpos a partir del día 15 postvacunación.
![]() Los 3 rayones expuestos a los vacunados también mostraron una respuesta positiva de anticuerpos a partir del día 14 tras el contacto.
Los 3 rayones expuestos a los vacunados también mostraron una respuesta positiva de anticuerpos a partir del día 14 tras el contacto.
 SUPERVIVENCIA Y LESIONES
SUPERVIVENCIA Y LESIONES
La respuesta inmunitaria de las jabatas vacunadas y expuestas fue capaz de protegerlas frente a la cepa Arm07 del VPPA:
![]() Tras el desafío con el virus, 11 de las 12 jabatas vacunadas y expuestas a la vacuna sobrevivieron (92% de supervivencia).
Tras el desafío con el virus, 11 de las 12 jabatas vacunadas y expuestas a la vacuna sobrevivieron (92% de supervivencia).
![]() Ninguno de estos 11 animales desarrolló síntomas o lesiones compatibles con la PPA tras el desafío (Imagen 1 A).
Ninguno de estos 11 animales desarrolló síntomas o lesiones compatibles con la PPA tras el desafío (Imagen 1 A).
En contraste, todos los animales control que recibieron una dosis del virus sin una inmunización previa desarrollaron severos síntomas clínicos compatibles con PPA (Imagen 1 B).
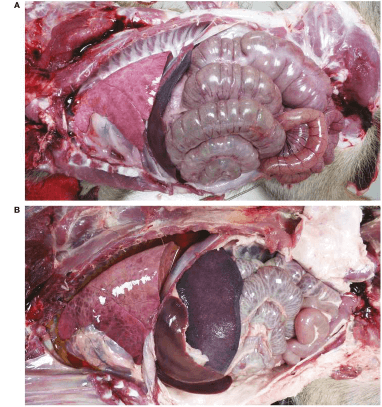
Imagen 1. Cavidad abdominal de (A) jabata vacunada por vía oral con la cepa Lv17/WB/Rie1 y (B) infectada con la cepa virulenta Arm07 de la VPPA por vía intramuscular (sin inmunización previa). El animal de la imagen (B) presenta hidrotórax, hepatomegalia y esplenomegalia.
 VIREMIA
VIREMIA
La determinación por PCR de la presencia del ADN vírico en los tejidos analizados confirmó la ausencia del virus en 3 de las jabatas vacunadas, mientras que las demás tuvieron resultados débilmente positivos.

Los resultados de este estudio demuestran que la vacunación oral con la cepa v17/WB/Rie1 ofrece una protección del 92% frente a la cepa virulenta Arm07 del VPPA.
Esta protección se traduce, no solo en la supervivencia de los animales, sino también en la ausencia de signos clínicos compatibles con la PPA, hallazgos patológicos y la presencia del virus en los órganos diana.
Este candidato vacunal podría ser la primera vacuna oral frente al genotipo II testado en jabalíes. Su uso en el campo permitiría:
 Reducir el número de animales susceptibles
Reducir el número de animales susceptibles
 Incrementar la inmunidad de grupo
Incrementar la inmunidad de grupo
 Reducir la incidencia de PPA
Reducir la incidencia de PPA
En el contexto actual, es necesario contar con todas las herramientas posibles para reforzar y rediseñar los planes de control de la PPA, especialmente teniendo en cuenta que, hasta ahora, ninguna de las medidas aplicadas en las poblaciones de jabalíes silvestres ha demostrado ser efectiva.
En el futuro será necesario examinar la seguridad de la vacuna cuando sea administrada de forma repetida o en caso de sobredosis, así como su estabilidad genética tras varios pases, su estabilidad en el campo y la forma de diferenciarla del virus de campo mediante las técnicas de análisis serológico DIVA.
[/registrados]
Suscribete ahora a la revista técnica porcina
AUTORES

Bioseguridad aplicada frente a Peste Porcina Africana: protocolos clave en granja, logística y control externo
David García Páez
Cómo cuidar la salud respiratoria de los cerdos: medidas clave
Alejandro Cid González Ana I. Pastor Calonge César B. Gutiérrez Martín Mario Delgado García Óscar Mencía-Ares Sonia Martínez Martínez
2026: consolidar fortalezas para avanzar con firmeza

Respuesta de emergencia en accidentes con transporte porcino: la experiencia danesa
Cecilie Kobek-Kjeldager Kirstin Dahl-Pedersen Mette S. Herskin
Microbiota intestinal en el cerdo: de la taxonomía a la función en producción porcina
Eduard de la Torre Candán
Energía neta y crecimiento porcino: claves para una mejor predicción
Gabriela Martínez
La apuesta ganadora de Porgaor, Grupo LANKA: el sistema de alimentación individualizada en maternidades, Materneo de Asserva

El arte de alimentar a cerdas reproductoras: inteligencia artificial al servicio de la nutrición y productividad
Gustavo Márquez Esteban Pablo Fuentes Pardo Sara Crespo Vicente
Lechones más fuertes y numerosos al destete

Estrategia nutricional active feeding en lechones destetados PRRS positivos
Alberto Morillo Alujas
MASTERFLY® BAIT: control eficaz y duradero de moscas

El destete como punto clave de la productividad: puntos críticos a tener en cuenta
Anabel Fernández Bravo Andrea Martínez Martínez Elena Goyena Salgado Emilio José Ruiz Fernández Francisco Frances Diaz José Manuel Pinto Carrasco Manuel Toledo Castillo Simón García Legaz
Medidas para el control de la cepa Rosalía de PRRS

Gestionar la incertidumbre cuando el miedo entra en la granja
Laura Pérez Sala
Bioseguridad y control: estrategias para afrontar el PRRS y PPA en un escenario de riesgo