Las aflatoxinas y la ocratoxina A son importantes micotoxinas que pueden contaminar el alimento que ingieren nuestros cerdos. ¿Qué consecuencias tiene su ingestión?
Las aflatoxinas y la ocratoxina A son importantes micotoxinas que pueden contaminar el alimento que ingieren nuestros cerdos. ¿Qué consecuencias tiene su ingestión?

Las aflatoxinas y la ocratoxina A son importantes micotoxinas que pueden contaminar el alimento que ingieren nuestros cerdos. ¿Qué consecuencias tiene su ingestión?
Aflatoxinas
Las aflatoxinas (AFs) son producidas principalmente por Aspergillus flavus, A. parasiticus y A. nomius, detectándose normalmente en maíz, cacahuetes y semillas de algodón.
Las AFs más comunes son AFB1, AFB2, AFG1 y AFG2.
La AFB1 se considera un hepatocarcinógeno activo y es el más importante en términos de toxicidad en porcino1, dado que el hígado es el principal órgano diana de la AFB1.
Las aflatoxinas, aparte de ser hepatotóxicas, tienen efectos mutagénicos y, posiblemente, teratogénicos en los animales, estando categorizados como carcinógenos humanos de Clase 1 por la Agencia Internacional de Investigaciones sobre el Cáncer (IARC).
| Asimismo, estas micotoxinas reducen la absorción de nutrientes y la ganancia de peso en los cerdos, mientras que la exposición crónica a dosis bajas resulta en ictericia (apariencia pálida-amarillenta del hígado) con puntos hemorrágicos en el hígado y niveles variables de fibrosis y cirrosis, necrosis centrolobulillar difusa y degeneración grasa2. |
 ¿Podemos observar efectos de las aflatoxinas sobre los parámetros reproductivos porcinos?
¿Podemos observar efectos de las aflatoxinas sobre los parámetros reproductivos porcinos?
 Pocos estudios relacionan las aflatoxinas con la reproducción porcina. Por ejemplo, el aborto no es de esperar en los casos de aflatoxicosis7.
Pocos estudios relacionan las aflatoxinas con la reproducción porcina. Por ejemplo, el aborto no es de esperar en los casos de aflatoxicosis7.
Cerdas reproductoras
No obstante, existen estudios que demuestran que la exposición de las cerdas reproductoras a aflatoxinas sí tiene efectos sobre sus lechones. Así, a pesar de que son capaces de tener una gestación y reproducción normal cuando son alimentadas con niveles de aflatoxinas entre 500 y 700 ppb, sus lechones muestran retraso en el crecimiento debido la excreción de aflatoxinas en leche3,4.
De forma similar, se ha observado una reducción en el peso de los lechones al nacimiento tras alimentar a las cerdas con pienso con 800 ppb de AFB1 durante la segunda mitad de la gestación y durante la lactación.

La exposición in vitro de los ovocitos a 50 μM AFB1 tiene efectos sobre su maduración debido a:
Modificaciones epigenéticas (incremento de los niveles de metilación)
![]() Inducción de estrés oxidativo
Inducción de estrés oxidativo
![]() Excesiva autofagia y apoptosis5
Excesiva autofagia y apoptosis5

Por otro lado, se ha observado que la AFB1 puede alterar el desarrollo embrionario temprano (la formación del blastocisto se puede ver alterada por el tratamiento con 1 nM de AFB1) debido a estrés oxidativo (exceso de especies de oxígeno reactivo), inducción de daños en el ADN, alteración de los mecanismos de reparación del ADN, inducción de la apoptosis y autofagia6.
Verracos
Con respecto a los verracos, se han asociado los efectos de las aflatoxinas con la eficiencia reproductiva7, encontrándose bajas concentraciones espermáticas, baja supervivencia de los espermatozoides y una mayor proporción de espermatozoides anormales simultáneamente con elevados niveles de AFB1 en plasma seminal.

Ocratoxina A
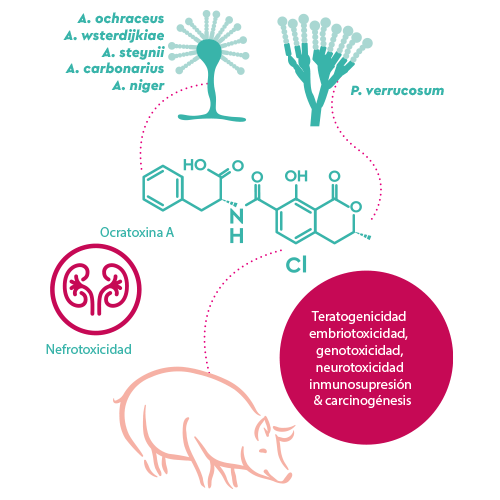
La ocratoxina A (OTA) es producida por varias especies de Aspergillus y Penicillium, como Penicillium verrucosum A.ochraceus, A. westerdijkiae, A.steynii, A. carbonarius y A. niger8.
| Su órgano diana primario son los riñones (nefrotoxicidad), aunque puede inducir varios efectos tóxicos como teratogenicidad, embriotoxicidad, genotoxicidad, neurotoxicidad, inmunosupresion y carcinogénesis8,9, habiendo sido clasificada por la IARC como posible carcinógeno humano (grupo 2B). |
 ¿Qué consecuencias tiene la Ocratoxina A sobre la reproducción porcina?
¿Qué consecuencias tiene la Ocratoxina A sobre la reproducción porcina?
Cerdas reproductoras
 Estudios in vitro han demostrado que la OTA afecta negativamente a la maduración de los ovocitos porcinos (reducida tasa de extrusión del corpúsculo polar de los ovocitos porcinos) con niveles de exposición superiores a 5 μM10.
Estudios in vitro han demostrado que la OTA afecta negativamente a la maduración de los ovocitos porcinos (reducida tasa de extrusión del corpúsculo polar de los ovocitos porcinos) con niveles de exposición superiores a 5 μM10.
Verracos
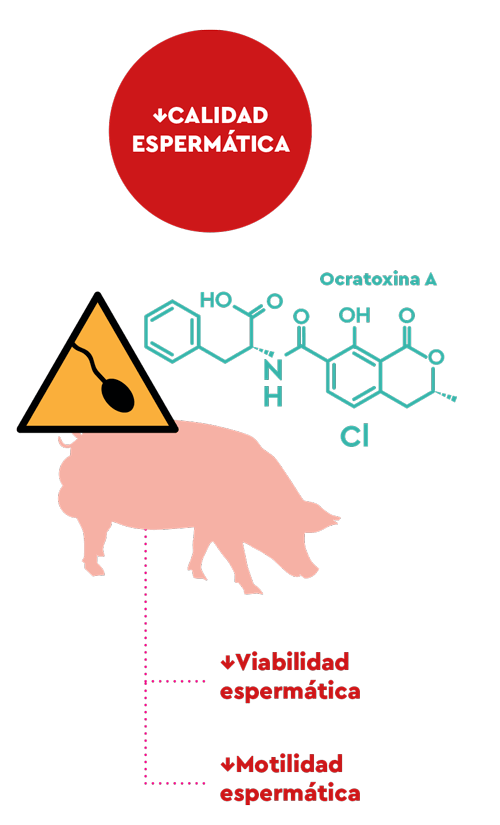
En un estudio con verracos (250 kg de peso) que recibieron 0,08 μg/kg de OTA por vía oral durante 6 semanas, se observó una reducción en la viabilidad espermática, motilidad inicial hacia delante y motilidad a las 24 horas de almacenamiento11.
| Asimismo, se ha sugerido que la administración de OTA a verracos en altas concentraciones podría afectar a la producción espermática y la calidad seminal de los verracos al reducir la motilidad inicial y la longevidad de los espermatozoides12. |
Artículo completo publicado en Mycotoxinsite:
Bibliografía
1. Doll S., Danicke S. The Fusarium toxins deoxynivalenol (DON) and zearalenone (ZON) in animal feeding. Prevent. Vet. Med. 2011, 102, 132– 145.
2. Ensley, S.M.; Radke, S.L. Mycotoxins in Grains and Feeds. In Disease of Swine, 11th ed.; Zimmerman, J.J.; Karriker, L.A.; Ramirez, A.; Schwartz, K.J., Stevenson, G.W.; Zhang, J. Eds.; Wiley-Blackwell, Hoboken, NJ, USA, 2019; pp. 1055–1071.
3. Armbrecht B.H., Wiseman H.G., Shalkop W.T. Swine aflatoxicosis. II. The chronic response in brood sows fed sublethal amounts of aflatoxin. Environ Physiol Biochem 1972, 2:77-85.
4. McKnight C.R., Armstrong W.D., Hagler W.M., Jones E.E. The effects of aflatoxin on brood sows and the newborn pigs. J Anim Sci 1983, 55(Suppl 1):104.
5. Liu J., Wang Q.C., Han J., Xiong B., Sun S.C. Aflatoxin B1 is toxic to porcine oocyte maturation. Mutagenesis 2015, 30(4):527-35.
6. Shin K-T., Guo J., Niu Y.-J., Cui X.-S. The toxic effect of aflatoxin B1 on early porcine embryonic development, Theriogenology 2018, 118, 157-163.
7. Picha J, Cerovsky J, Pichova D (1986) Fluctuation in the concentration of sex steroids and aflatoxin B1 in the seminal plasma of boars and its relation to sperm production. Vet Med 1986, 31:347-357.
8. Klarić MS, Rašić D, Peraica M. Deleterious effects of mycotoxin combinations involving ochratoxin A. Toxins 2013, 5(11):1965-87.
9. Yang S, Zhang H, De Saeger S, De Boevre M, Sun F, Zhang S, Cao X., Wang Z. In vitro and in vivo metabolism of ochratoxin A: a comparative study using ultra-performance liquid chromatography-quadrupole/time-of-flight hybrid mass spectrometry. Anal Bioanal Chem 2015, 407(13):3579-89.
Suscribete ahora a la revista técnica porcina
AUTORES

Es momento de atraer y retener talento
Laura Pérez Sala
Foro Porcino Aragón INTERPORC

Influencia del método de aplicación de productos de hierro y anticoccidios en el comportamiento de lechones lactantes y en los factores asociados a estrés
Antonio González-Bulnes Daniel Sperling Gonzalo Díaz-Amor Hamadi Karembe Joaquín Morales María Rodríguez
Ventilación en granjas porcinas: clave para el bienestar y la productividad
Laura Batista
PRAN 2025-2027: Una estrategia integral para preservar la salud pública, animal y ambiental
Cristiana Teixeira Justo Cristina Muñoz Madero María Vilar Ares
Bioseguridad porcina 360°: de las barreras visibles a los reservorios ocultos – Parte I
David García Páez
Nutrición porcina: aliado clave en la evolución de la industria
Cerdas hiperprolíficas: ¿pueden coexistir el rendimiento y el bienestar?

Desarrollo de indicadores fisiológicos y conductuales de estado emocional positivo en cerdos
Emma Fàbrega i Romans Liza Moscovice Marc Bagaria
El papel del enriquecimiento ambiental en la mejora del bienestar y rendimiento zootécnico en porcino

Proteger frente al virus PRRS – Cepa Rosalia
Clara Farré Ester Maiques Javier Abadías Jonás Hernández
Digitalización, predicción y compromiso con la sociedad en la producción porcina
Cristina Sanmartín Ruiz Gonzalo Cano García José Ángel Fernández Ortiz Monse Suarez
Evolución en la alimentación de los destetes: el sistema iQon Multifast™ lo hace posible

Vacunación: herramienta decisiva en la prevención del PRRS y Circovirus Porcino tipo 2

Acidificación del agua en transición porcina: salud intestinal y producción

Decálogo para alcanzar la excelencia en granjas de producción porcina
Anabel Fernández Bravo Andrea Martínez Martínez Elena Goyena Salgado Emilio José Ruiz Fernández José Manuel Pinto Carrasco Manuel Toledo Castillo Simón García Legaz