 Actualmente, es imposible aislar y caracterizar todas las bacterias mediante el cultivo bacteriológico, pero gracias a los avances de las técnicas moleculares como la secuenciación masiva, se pueden caracterizar grupos específicos de bacterias.
Actualmente, es imposible aislar y caracterizar todas las bacterias mediante el cultivo bacteriológico, pero gracias a los avances de las técnicas moleculares como la secuenciación masiva, se pueden caracterizar grupos específicos de bacterias.
El intestino del cerdo alberga un conjunto de bacterias que conforman una estructura extremadamente compleja que se ve alterada fácilmente por numerosos factores.

En el intestino del cerdo se encuentran alrededor de 100 billones de bacterias (1.000 especies). Este conjunto de bacterias se denomina microbiota.
En cada fase de producción del animal, esta microbiota es diferente. No solo varía dependiendo de la edad del animal, sino que en cada tramo del intestino vamos a encontrar diferencias tanto cualitativas como cuantitativas. Es decir, estamos ante una estructura extremadamente compleja que se ve alterada fácilmente por numerosos factores.
 Actualmente, es imposible aislar y caracterizar todas las bacterias mediante el cultivo bacteriológico, pero gracias a los avances de las técnicas moleculares como la secuenciación masiva, se pueden caracterizar grupos específicos de bacterias.
Actualmente, es imposible aislar y caracterizar todas las bacterias mediante el cultivo bacteriológico, pero gracias a los avances de las técnicas moleculares como la secuenciación masiva, se pueden caracterizar grupos específicos de bacterias.
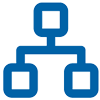 La taxonomía se basa en agrupar las bacterias desde un amplio espectro conocido como reino hasta el espectro más reducido que se denomina especie. Los estudios de investigación suelen trabajar con el filo y el género.
La taxonomía se basa en agrupar las bacterias desde un amplio espectro conocido como reino hasta el espectro más reducido que se denomina especie. Los estudios de investigación suelen trabajar con el filo y el género.
Lo que se está utilizando en la actualidad son las OTU (Operational Taxonomic Unit). Estas OTU se refieren básicamente al género bacteriano. Se ha conseguido alcanzar una calidad en los métodos de diagnóstico, de tal forma que ya podemos discernir entre géneros.
Una vez identificado el género, es cierto que determinar la especie es cualitativamente muy difícil, aunque no imposible. No obstante, podemos obtener información taxonómica (de forma ascendente) hasta llegar al reino, obteniendo así una información más global.
 Características generales de la microbiota intestinal del cerdo
Características generales de la microbiota intestinal del cerdo
Existen bacterias comensales y beneficiosas en el intestino, además de bacterias patógenas.
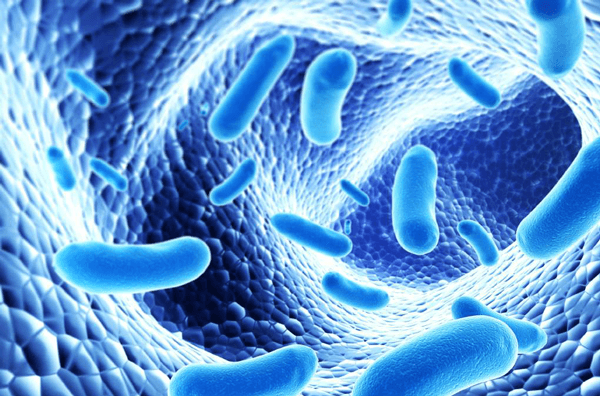
A modo de conocimiento para situar cada especie en su lugar, se esquematiza a continuación dónde se colocaría cada una de las especies más conocidas.
En un cerdo sano, se sabe que los filos más prevalentes son Firmicutes y Bacteroidetes. Estos dos filos suponen más del 90% de la población.
 Los géneros más prevalentes de Firmicutes son los Clostridiales (la mayoría son bacterias comensales que no causan patogenicidad como Clostridium butyricum) y los Bacilli. En el caso de Bacteroidetes son Bacteroides y Prevotella.
Los géneros más prevalentes de Firmicutes son los Clostridiales (la mayoría son bacterias comensales que no causan patogenicidad como Clostridium butyricum) y los Bacilli. En el caso de Bacteroidetes son Bacteroides y Prevotella.
Hay que tener en cuenta que aunque estos dos filos constituyan un alto porcentaje de la microbiota intestinal, existen otros filos de especial importancia como Proteobacteria, la cual incluye a todas las enterobacterias (E.coli, Salmonella…), Actinobacteria, Spirochaetes y Verrucomicrobia.
Diversidad de la microbiota en función de la fase productiva
Como ya se ha mencionado, la microbiota intestinal varía dependiendo de la fase de producción en la que se encuentre el animal. La Figura 3 refleja esta ordenación.
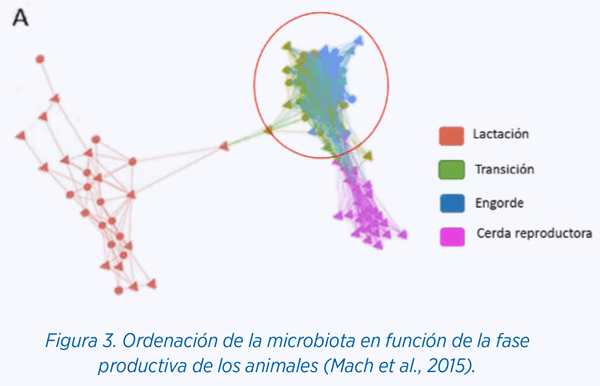

 Cabe destacar que durante la fase de lactación la microbiota de los lechones es más homogénea y, además, el número de especies diferentes (riqueza) es inferior. Esto se debe fundamentalmente al tipo de alimentación que reciben durante sus primeros días de vida (leche materna).
Cabe destacar que durante la fase de lactación la microbiota de los lechones es más homogénea y, además, el número de especies diferentes (riqueza) es inferior. Esto se debe fundamentalmente al tipo de alimentación que reciben durante sus primeros días de vida (leche materna).
![]() Ya desde esta fase se diferencian los dos filos anteriormente mencionados como los más prevalentes. Respecto a Proteobacteria, su proporción puede alcanzar el 15% del total de la microbiota. La bacteria principal es E.coli, la cual puede llegar a alcanzar el 5%.
Ya desde esta fase se diferencian los dos filos anteriormente mencionados como los más prevalentes. Respecto a Proteobacteria, su proporción puede alcanzar el 15% del total de la microbiota. La bacteria principal es E.coli, la cual puede llegar a alcanzar el 5%.
Pero, ¿qué ocurre tras el destete? 
 Tanto el sistema digestivo como el sistema inmune van a sufrir una serie de alteraciones y suele coincidir con que la edad de los animales no es la idónea para que el proceso de destete se desarrolle con normalidad. El periodo de lactación en la naturaleza tiene una duración de unas 20 semanas (Jensen et al., 1992; Weary et al., 2007).
Tanto el sistema digestivo como el sistema inmune van a sufrir una serie de alteraciones y suele coincidir con que la edad de los animales no es la idónea para que el proceso de destete se desarrolle con normalidad. El periodo de lactación en la naturaleza tiene una duración de unas 20 semanas (Jensen et al., 1992; Weary et al., 2007).
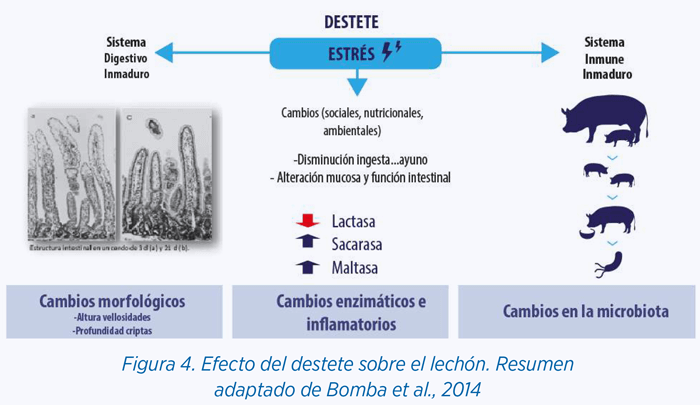
Aparte de los cambios morfológicos, enzimáticos e inflamatorios del intestino, tras el destete se va a producir un cambio en la propia microbiota intestinal, la cual es la responsable de numerosas funciones (digestión y fermentación de carbohidratos, producción de vitaminas, regulación de la respuesta inmune…). Destaca la pérdida de unos filos y el aumento de otros. Por ejemplo, Proteobacteria y Fusobacteria disminuyen tras el destete (Chen et al., 2017).
Tras el destete abundan las bacterias anaerobias estrictas como el grupo de los Clostridiales y de Prevotella.
 Cuando las condiciones son beneficiosas, es decir, con abundancia de anaerobios estrictos, productores de ácidos grasos de cadena corta, presencia limitada de oxígeno, etc., se previene la expansión de patógenos como Salmonella.
Cuando las condiciones son beneficiosas, es decir, con abundancia de anaerobios estrictos, productores de ácidos grasos de cadena corta, presencia limitada de oxígeno, etc., se previene la expansión de patógenos como Salmonella.

Se ha establecido que durante esta fase se pueden distinguir dos tipos de enterotipos (perfil de microbiota que se repite en un grupo de individuos).
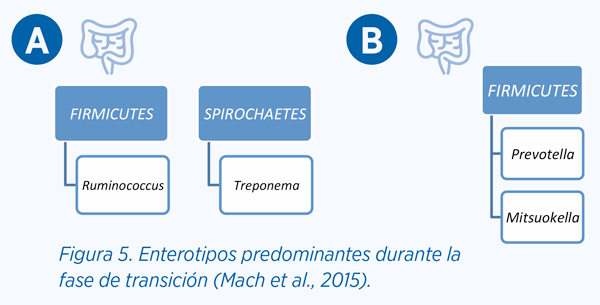
 No se conocen los mecanismos exactos de por qué en unos animales se desarrolla un enterotipo específico y en otros animales otro. Pero está claro que hay que mantener un equilibrio entre los diferentes microorganismos, sobre todo cuando en los diferentes tramos intestinales escasean los nutrientes.
No se conocen los mecanismos exactos de por qué en unos animales se desarrolla un enterotipo específico y en otros animales otro. Pero está claro que hay que mantener un equilibrio entre los diferentes microorganismos, sobre todo cuando en los diferentes tramos intestinales escasean los nutrientes.
Sería interesante conseguir un aumento de la diversidad de microbiota beneficiosa con el fin de que los microorganismos que se consideran patógenos tengan menos oportunidades de colonizar la mucosa intestinal.
Efecto de microorganismos patógenos sobe la microbiota intestinal del cerdo
 Hasta ahora, se ha visto que el uso de antibióticos y de óxido de zinc ha controlado la mayoría de procesos digestivos que ocurren tras el destete. Actualmente, prestando atención a los principales problemas digestivos que ocurren durante la fase de transición, se observa un aumento de patologías digestivas como la diarrea postdestete causada por Escherichia coli enterotoxigénico (ETEC).
Hasta ahora, se ha visto que el uso de antibióticos y de óxido de zinc ha controlado la mayoría de procesos digestivos que ocurren tras el destete. Actualmente, prestando atención a los principales problemas digestivos que ocurren durante la fase de transición, se observa un aumento de patologías digestivas como la diarrea postdestete causada por Escherichia coli enterotoxigénico (ETEC).
 Hay un elevado porcentaje de estos casos de diarrea que se están dando hoy en día, que no siguen el típico patrón de diarrea asociada al propio destete, sino que son procesos diarreicos más tardíos que coinciden con el cambio de pienso en esta fase de producción.
Hay un elevado porcentaje de estos casos de diarrea que se están dando hoy en día, que no siguen el típico patrón de diarrea asociada al propio destete, sino que son procesos diarreicos más tardíos que coinciden con el cambio de pienso en esta fase de producción.
Principalmente, se achaca a la reducción del uso de antibióticos en pienso, así como a la retirada del óxido de zinc.
Esta retirada está siendo paulatina y ya hay un elevado número de granjas que trabajan sin óxido de zinc en los piensos stárter, mientras que permanece en el prestárter durante un periodo de tiempo más prolongado. Es en este momento de cambio de pienso cuando aparecen casos de diarrea colibacilar debida en un alto porcentaje a ETEC.

 Hay que tener en cuenta que cualquier alteración de microorganismos comensales puede influenciar tanto la patología gastrointestinal (Zhang et al., 2015) como la eficacia de las vacunas (Nakaya et al., 2015). Patógenos como E.coli enterotoxigénico, Salmonella o Brachyspira hyodysenteriae, producen cambios en la microbiota intestinal durante la infección. El mayor impacto de estos cambios se produce en el lugar donde actúa el microorganismo.
Hay que tener en cuenta que cualquier alteración de microorganismos comensales puede influenciar tanto la patología gastrointestinal (Zhang et al., 2015) como la eficacia de las vacunas (Nakaya et al., 2015). Patógenos como E.coli enterotoxigénico, Salmonella o Brachyspira hyodysenteriae, producen cambios en la microbiota intestinal durante la infección. El mayor impacto de estos cambios se produce en el lugar donde actúa el microorganismo.
 Respecto a E. coli se han evidenciado cambios en la microbiota tras una infección por el mismo.
Respecto a E. coli se han evidenciado cambios en la microbiota tras una infección por el mismo.
 En 2018, Pollock evidenció que, tras la infección controlada de E. coli F4 en lechones durante el periodo postdestete, los cerdos sufren un cambio de microbiota fecal, la cual se encuentra relacionada con la excreción de E. coli. Es decir, en el día 8 postdestete aquellos cerdos infectados de E. coli F4, que excretaban una elevada cantidad de E. coli en heces, contenían una comunidad de microorganismos significativamente diferente a aquellos cerdos control que no excretaban la bacteria.
En 2018, Pollock evidenció que, tras la infección controlada de E. coli F4 en lechones durante el periodo postdestete, los cerdos sufren un cambio de microbiota fecal, la cual se encuentra relacionada con la excreción de E. coli. Es decir, en el día 8 postdestete aquellos cerdos infectados de E. coli F4, que excretaban una elevada cantidad de E. coli en heces, contenían una comunidad de microorganismos significativamente diferente a aquellos cerdos control que no excretaban la bacteria.
 Por otro lado, aquellos cerdos que habían sido infectados por E. coli F4, pero que excretaban una cantidad muy baja del mismo, contenían una microbiota muy similar a los cerdos control.
Por otro lado, aquellos cerdos que habían sido infectados por E. coli F4, pero que excretaban una cantidad muy baja del mismo, contenían una microbiota muy similar a los cerdos control.
Además, se observó que aquellos cerdos infectados que ya no excretaban la bacteria a los 12 y 19 días postdestete, portaban una microbiota significativamente diferente a los que también se habían infectado por la bacteria y sí que seguían excretándola en las heces.
Se han barajado múltiples factores que contribuyen a que unos cerdos excreten durante más tiempo la bacteria y una de esas opciones es el tema de la exclusión competitiva que se da entre E. coli patógena y el resto de microbiota. Sobre todo, hay que tener en cuenta que en un ambiente donde escasean los nutrientes, va a ocurrir este proceso de exclusión.
![]() Interacción entre la microbiota intestinal del cerdo y el uso de vacunas vivas orales
Interacción entre la microbiota intestinal del cerdo y el uso de vacunas vivas orales
Prestando atención al uso de vacunas vivas orales cuyo mecanismo de acción contribuye a mantener la integridad intestinal, se ha intentado buscar la existencia de una relación con la microbiota del intestino.
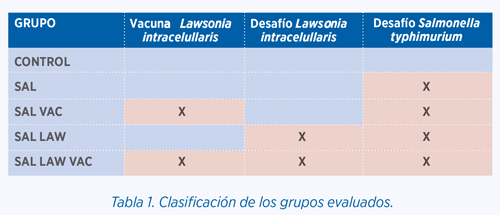
Es el caso del estudio publicado por Leite y cols. en 2018. En este estudio se evaluó el papel de una vacuna viva oral atenuada de Lawsonia intracellularis.
Este patógeno puede aumentar tanto la susceptibilidad como la excreción de Salmonella entérica. El estudio dividió a los animales en diferentes grupos en función de tres factores (vacunación/no vacunación frente a L. intracellularis, infección/no infección de L. intracellularis, infección/no infección de S. Typhimurium).
 Uno de los hallazgos a tener en cuenta ocurrió a los 7 días postinfección con S. typhimurium. En el grupo Sal Law Vac se observó que solo el 38% de los cerdos excretaban Salmonella en heces. Sin embargo, el resto de grupos excretaron en un 100% la bacteria. En la Tabla 2 se refleja el porcentaje de excreción en heces de Salmonella en función del grupo.
Uno de los hallazgos a tener en cuenta ocurrió a los 7 días postinfección con S. typhimurium. En el grupo Sal Law Vac se observó que solo el 38% de los cerdos excretaban Salmonella en heces. Sin embargo, el resto de grupos excretaron en un 100% la bacteria. En la Tabla 2 se refleja el porcentaje de excreción en heces de Salmonella en función del grupo.
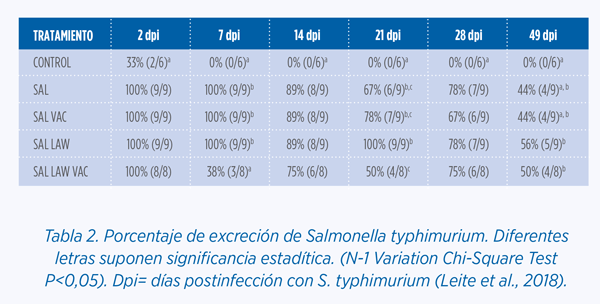
Para explicar la reducción de la excreción de Salmonella tras la vacunación oral de L. intracellularis, estudiaron el microbioma intestinal, que se ve alterado en presencia de S. enterica (Kim et al., 2017).
En el grupo Sal Law Vac se observó un aumento de Clostridium butyricum. Esta bacteria puede reducir la susceptibilidad de la infección por Salmonella. De esta forma, se da una idea de la eficacia indirecta que tiene la vacunación frente a L. intracellularis en el control de la infección por Salmonella.
Respecto al tipo de poblaciones de la microbiota intestinal, el aumento de lactobacillus se puede asociar al incremento de la virulencia y excreción de S. typhimurium (Drumo et al., 2106). En este caso, el grupo Sal Law Vac obtuvo una menor proporción de Lactobacillus. Esto podría explicarse si se tiene en cuenta que fueron vacunados de L. intracellularis y, la vacunación, puede inducir un cambio en la composición del microbioma.

Este tipo de estudios aportan información y dan ideas acerca de la búsqueda de la interacción entre la microbiota intestinal y las herramientas de control que existen hoy en día para mantener la integridad del intestino.
 El uso de la metagenómica va a ser importante para los próximos años, ya que como se está viendo, se puede analizar el impacto que tienen diferentes medidas de control sobre la microbiota intestinal de los animales. Por tanto, todo aquello que se encuentra ya en el mercado cuya función básica es la de aportar salud intestinal (vacunas, probióticos, prebióticos…), puede ser evaluado desde el punto de vista de la microbiota intestinal.
El uso de la metagenómica va a ser importante para los próximos años, ya que como se está viendo, se puede analizar el impacto que tienen diferentes medidas de control sobre la microbiota intestinal de los animales. Por tanto, todo aquello que se encuentra ya en el mercado cuya función básica es la de aportar salud intestinal (vacunas, probióticos, prebióticos…), puede ser evaluado desde el punto de vista de la microbiota intestinal.
EM-ES-19-0028
Suscribete ahora a la revista técnica porcina
AUTORES

Bioseguridad aplicada frente a Peste Porcina Africana: protocolos clave en granja, logística y control externo
David García Páez
Cómo cuidar la salud respiratoria de los cerdos: medidas clave
Alejandro Cid González Ana I. Pastor Calonge César B. Gutiérrez Martín Mario Delgado García Óscar Mencía-Ares Sonia Martínez Martínez
2026: consolidar fortalezas para avanzar con firmeza

Respuesta de emergencia en accidentes con transporte porcino: la experiencia danesa
Cecilie Kobek-Kjeldager Kirstin Dahl-Pedersen Mette S. Herskin
Microbiota intestinal en el cerdo: de la taxonomía a la función en producción porcina
Eduard de la Torre Candán
Energía neta y crecimiento porcino: claves para una mejor predicción
Gabriela Martínez
La apuesta ganadora de Porgaor, Grupo LANKA: el sistema de alimentación individualizada en maternidades, Materneo de Asserva

El arte de alimentar a cerdas reproductoras: inteligencia artificial al servicio de la nutrición y productividad
Gustavo Márquez Esteban Pablo Fuentes Pardo Sara Crespo Vicente
Lechones más fuertes y numerosos al destete

Estrategia nutricional active feeding en lechones destetados PRRS positivos
Alberto Morillo Alujas
MASTERFLY® BAIT: control eficaz y duradero de moscas

El destete como punto clave de la productividad: puntos críticos a tener en cuenta
Anabel Fernández Bravo Andrea Martínez Martínez Elena Goyena Salgado Emilio José Ruiz Fernández Francisco Frances Diaz José Manuel Pinto Carrasco Manuel Toledo Castillo Simón García Legaz
Medidas para el control de la cepa Rosalía de PRRS

Gestionar la incertidumbre cuando el miedo entra en la granja
Laura Pérez Sala
Bioseguridad y control: estrategias para afrontar el PRRS y PPA en un escenario de riesgo