La etiología de las pérdidas de gestación en cerdas puede ser muy amplia, abarcando problemas de tipo infeccioso o no infeccioso, con la implicación del manejo, alimentación, ambiente físico y climático, higiene, etc.

Las pérdidas de gestación pueden darse en cualquier momento y pueden ser totales o parciales.
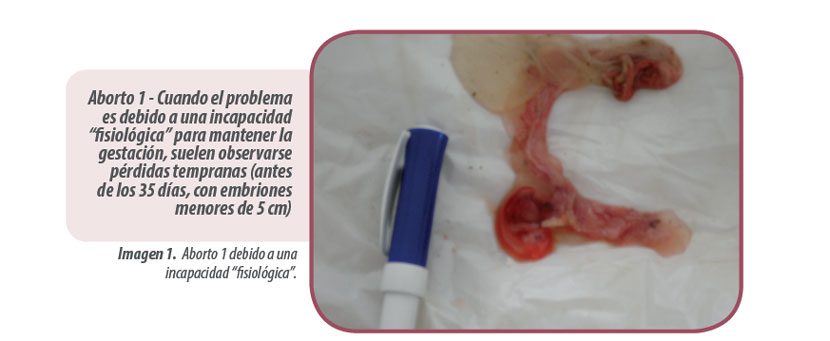
A partir de los 35 días de gestación suelen acabar en un aborto visible, mientras que con anterioridad pueden ser más difíciles de detectar o pueden dar lugar a reabsorciones.
Provocarán una pérdida de prolificidad, o el nacimiento de lechones momificados si la muerte fetal ha ocurrido a partir de los 35 días de gestación.
Podemos clasificar los tipos de pérdidas en 3 apartados:
Los embriones participan activamente en su propio desarrollo, un número reducido de embriones y/o de baja calidad compromete su propia supervivencia.
Alrededor del día 13, los oocitos fertilizados deben implantarse.
Si en este momento su calidad o número es bajo (5 o menos), los embriones implantan, pero su capacidad para producir progesterona y otros factores que mantienen la gestación será insuficiente.
Esto desencadenará una mortalidad embrionaria progresiva, resultando en una repetición acíclica (habitualmente entre 24-30 días).
A partir del día 35 de gestación el embrión empieza a osificar y pasamos a llamarle feto. En este momento ya es lo suficientemente grande para mantener la gestación aunque el número de fetos sea menor de 5.
Así pues, es posible que una cerda acabe pariendo tan solo un lechón.
| Fallo | Resultado |
| No hay ovulación | Anoestro |
| No hay fertilización | Repetición cíclica (21 días) |
| Mortalidad embrionaria (>10 días) | Repetición cíclica (21 días) |
| Sólo 5 embriones o menos presentes el día 10 | Muerte progresiva, repetición acíclica (24-38 días) |
| Implantación, pero muerte de todos los embriones antes del día 35 | Repetición acíclica (24-38 días) |
| 1-2 embriones sobreviven después del día 35 | Camada con 1-2 lechones nacidos |
| Todos los embriones mueren después del día 35 | Aborto o parto con lechones momificados |
La calidad de los folículos preovulatorios depende de muchos factores pero los más importantes son:
Podríamos escribir un artículo entero sobre estos factores, que básicamente pueden resumirse en cómo y cuándo estamos cubriendo las cerdas.
El “cómo” sería el tipo de técnica que se emplea, tiempo dedicado, estímulo del macho, la calidad del semen empleado, etc.
El “cuándo” sería la pauta de inseminación (en qué momento empieza y termina y cada cuándo se realiza).
Un ejemplo que explica claramente este punto es el uso de un semen de baja calidad. Si el semen es tan poco viable (semen totalmente muerto) que no logra fertilizar ningún oocito, el resultado será una repetición cíclica puesto que la concepción fracasará totalmente.
Sin embargo, si el semen es de baja calidad, pero con cierta capacidad fertilizante, el resultado será que un porcentaje menor de oocitos será fecundado. En esta situación, algunas cerdas pueden quedar preñadas pariendo menos lechones, otras pueden repetir de forma cíclica y otras pueden hacerlo de forma acíclica.
Estas últimas serían cerdas que alrededor del día 13 de gestación han logrado implantar un número limitado de embriones, lo que provoca su muerte paulatina a los pocos días y su salida en celo fuera de tiempo. Otras dos causas de fallo reproductivo que podríamos englobar dentro de este apartado son la intoxicación por micotoxinas estrogénicas (zearalenona) y la intoxicación por CO.
La zearalenona interfiere en la concepción e implantación provocando infertilidad y mortalidad embrionaria y de forma muy ocasional, abortos.
Existen muchos factores tanto infecciosos como no infecciosos que generan mortalidad embrionaria.
La mortalidad embrionaria pueden traducirse en pérdidas de prolificidad si la pérdida es parcial, o en repeticiones (tanto cíclicas como acíclicas) si la pérdida es total. Es probable que la reducción en prolificidad de la mayoría de explotaciones sea con más frecuencia debida a los efectos negativos sobre la supervivencia embrionaria que a una baja ovulación.
Un estado metabólico deficiente junto con una alimentación escasa durante el primer tercio de gestación puede desencadenar mortalidad embrionaria, más aún en casos de ambientes fríos (<16ºC) y corrientes de aire.
Existen factores que pueden incidir sobre más de uno de estos 3 puntos. Como hemos visto, un estado metabólico comprometido tiene efectos directos sobre la mortalidad embrionaria, pero también indirectos porque tiene efectos negativos sobre la ovulación.
Otro factor relevante en nuestro país, que afecta a la capacidad fisiológica para mantener la gestación incidiendo en diversos puntos simultáneamente es la infertilidad estacional. Por un lado, los efectos del fotoperiodo inciden sobre la regresión de los cuerpos lúteos. Por el otro, el efecto del calor incide en el consumo y en el estado metabólico de las cerdas.
Cualquier proceso que curse con dolor, inflamación o estrés tiene la capacidad de causar la pérdida de gestación.
La descarga aguda de citoquinas proinflamatorias (interferón-α, factor necrosis tumoral-α, il-1) conducte a liberación de cortisol y a una cascada hormonal que acaba con la liberación de prostaglandinas.
Los procesos inflamatorios crónicos, como las cojeras, otitis, quemaduras solares, cistitis y pielonefritis, parasitaciones extensas, lesiones dolorosas (en orejas, pezuñas, etc.) pueden inducir el aborto.
Las situaciones estresantes, (la competencia por la comida o agua, las altas densidades, las mezclas de animales, los suelos resbaladizos, las condiciones ambientales deficientes, los pinchazos, etc.) también pueden provocar problemas principalmente alrededor del momento de la implantación y especialmente al mezclar cerdas en patios con pocos días de gestación.
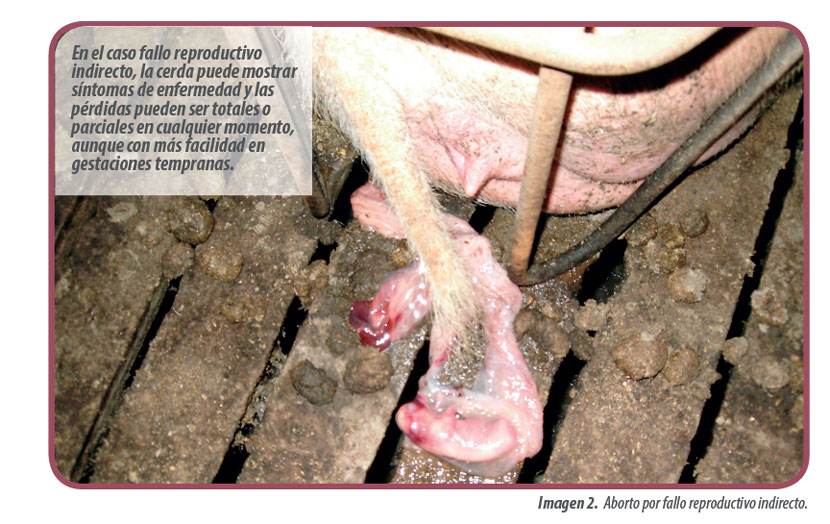
También hay procesos infecciosos que provocan enfermedad generalizada en la cerda y que potencialmente pueden acabar desencadenando la pérdida de la gestación en cualquier momento.
En principio, cualquier enfermedad de gravedad que afecte a la cerda tiene el potencial de inducir la pérdida de la gestación. Por ejemplo, un brote de Actinobacillus pleuropneumoniae o en algunos de los casos de diarrea epidémica que estamos viendo recientemente, es posible tener abortos en las cerdas afectadas de forma más severa.
Sin embargo, esto son situaciones puntuales. Las enfermedades más importantes que estarían afectando de forma recurrente dentro de este grupo, serían influenza, prrs, Mal rojo y otras que deberíamos considerar minoritarias, como el Aujeszky, la PPC o la PPA.
Las reacciones vacunales podrían también incluirse dentro de este grupo. una vacunación no deja de ser una infección más o menos controlada. Probablemente el PRRS sea un agente que actúe con más frecuencia provocando un aborto por causa directa (afectando directamente al feto y placenta). En este caso el resultado suele ser un aborto tardío o el nacimiento de lechones muertos y débiles. Sin embargo, los efectos sistémicos del PRRS en la cerda también tienen el potencial de provocar la pérdida de gestación por causa indirecta en cualquier momento.
Los síntomas en estos casos se centran en la cerda como consecuencia de los efectos sistémicos. Las cerdas mostrarán depresión, anorexia, fiebre (>39,5ºC) e incluso muerte. El aborto en estos casos suele ser un proceso rápido por lo que los fetos abortados son frescos, no muestran signos de descomposición y son firmes debido al rigor mortis.
Cuando vemos a la cerda enferma, la infección fetal es poco probable. Por este motivo el diagnóstico debe centrarse en la madre. Si tomamos muestras en la fase aguda de la enfermedad es posible que seamos capaces de detectar el antígeno mediante PCR en sangre en el caso de PRRS, en escobillón nasal, pulmón o fluidos orales. En el caso de influenza o mediante hemocultivo o aislamiento en varios tejidos en el caso del Mal rojo.
En casos de fallo reproductivo indirecto, la seroconversión en muestras pareadas casi siempre debería tener éxito, aunque deben tenerse en cuenta una serie de principios:
Esto significa que es posible que ya no veamos con tanta frecuencia a los animales afectados mostrando síntomas clínicos claros, ni que la enfermedad afecte a múltiples animales al mismo tiempo.
Por este motivo, frente a cualquier problema reproductivo en cerdas con signos de enfermedad, debemos pensar en Influenza como una de las posibles causas, pero si no vemos síntomas, tampoco la podemos descartar. Lo mismo sucedería con el Mal Rojo y el PRRS porque ambas enfermedades pueden presentarse de forma subclínica.
En este caso la infección se centra en el tracto genital , tejidos embrionarios-fetales o placenta.
Al afectar a la unión fetoplacental, la pérdida de gestación no suele ser consecuencia de un proceso agudo, sino de un proceso progresivo que puede acabar con la muerte de algunos (nacimiento de fetos momificados) o todos los fetos (aborto).
Entre el primer y segundo día de vida, el agente infeccioso suele replicarse en el tejido local.
A partir de aquí ocurre la diseminación en sangre (viremia o bacteremia) infectando a los fetos (frecuentemente solo algunos) y la difusión de la enfermedad a nivel de útero y entre fetos.
Esto suele desencadenar una pérdida de la gestación, habitualmente a partir de las 2 semanas post-infección.
Por este motivo, en este caso, la cerda no suele mostrar signos de enfermedad en el momento del aborto y los fetos aparecen auto líticos, blandos y sin rigor mortis.
La cerda no suele tener sintomatología clínica ni mostrar viremia o bacteriemia en el momento del aborto.
Incluso es posible que ya haya seroconvertido en el momento del aborto, por lo que no siempre detectaremos cambios en títulos significativos al tomar muestras pareadas.
El organismo debería ser detectable en placenta y /o fetos.
Es importante tenir en cuenta que no todos los fetos pueden estar infectados en el momento del aborto, por lo que es recomendable realizar un muestreo de 4 a 6 fetos por camada.
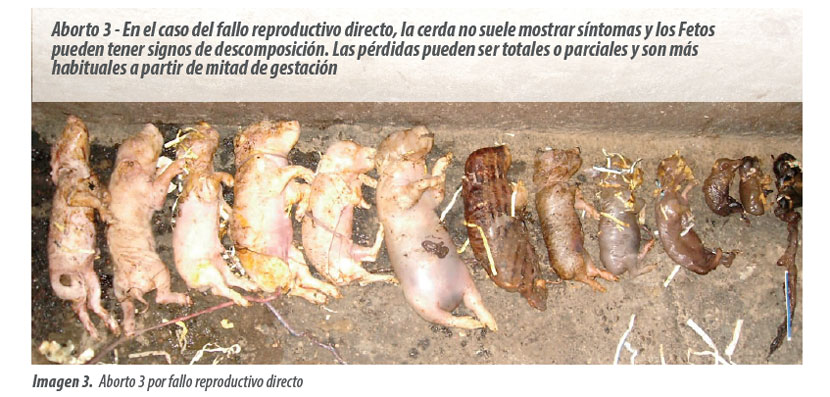
Entre las enfermedades infecciosas más importantes que inducen fallo reproductivo directo se encuentran el PRRS, Leptospirosis, Parvovirus, PCV2, Teschovirus – Enterovirus, Brucella y Chlamidia.
En el caso de la leptospirosis, la patogenia aún no está clara. Es posible que el efecto directo de la infección transplacental no sea la única causa, puesto que también existe un posible efecto indirecto de la bacteremia que cursa con síntomas poco claros en cerdas (puede haber fiebre, anorexia, depresión), aunque habitualmente estos síntomas no son detectados.
En el caso de Parvovirus, PCV2, Teschovirus – Enterovirus, son agentes que no se replican ampliamente en tejidos endometriales, no lesionan la placenta y tienen unan lenta diseminación entre fetos.
Por este motivo, el aborto no suele ser el resultado de esta infección, sino que más bien las cerdas afectades tienen mortinatos, momificados, mortalidad embrionaria (baja prolificidad) e infertilidad.
Las pérdidas de gestación pueden ser debidas a múltiples factores tanto infecciosos como no infecciosos, por lo que su diagnóstico y resolución no siempre son una tarea fácil.
Habitualmente será necesario combinar la interpretación de datos productivos, con la observación de síntomas y el uso de análisis laboratoriales para hallar la solución.
| Factores | Efectos | |
| Incapacidad “fisiológica” de mantener la gestación | Estado metabólico deficiente precubrición y/o en el primer tercio de gestación. Empeoramiento en ambientes fríos (<16ºC) y con corrientes de aireDuración lactación cortaFalta de estímulo machoPautas de fecundación inapropiadasMicotoxinasInfertilidad estacional | Principalmente inducen baja prolificidad /pérdidas tempranas (<35 días) |
| Fallo reproductivo indirecto | Procesos dolorosos, inflamación: cojeras, otitis, quemaduras solares, cistitis y pielonefritis, parasitaciones extensas, lesiones dolorosas (en orejas, pezuñas)…Estrés: competencia por la comida / agua, altas densidades, mezclas animales, suelos resbaladizos, condiciones ambientales deficientes, pinchazos procesos infecciosos: influenza, PRRS, Mal rojo, Aujeszky, PPC, PPAReacciones vacunales | La cerda puede mostrar síntomas de enfermedad. Potencial para provocar pérdidas totales o parciales en cualquier momento, aunque con más facilidad en gestaciones tempranas |
| Fallo reproductivo directo | Procesos infecciosos: PRRS, leptospirosis, Parvovirus, PCV2, Teschovirus – Enterovirus, Brucella y Chlamidia | Fetos con signos de descomposición, pérdidas totales o parciales más habituales a partir de mitad de gestación |
Suscribete ahora a la revista técnica porcina
AUTORES

El destete como punto clave de la productividad: puntos críticos a tener en cuenta
Anabel Fernández Bravo Andrea Martínez Martínez Elena Goyena Salgado Emilio José Ruiz Fernández Francisco Frances Diaz José Manuel Pinto Carrasco Manuel Toledo Castillo Simón García Legaz
2026: consolidar fortalezas para avanzar con firmeza

Energía neta y crecimiento porcino: claves para una mejor predicción
Gabriela Martínez
Estrategia nutricional active feeding en lechones destetados PRRS positivos
Alberto Morillo Alujas
Bioseguridad aplicada frente a peste porcina africana: protocolos clave en granja, logística y control externo
David García Páez
Microbiota intestinal en el cerdo: función en producción porcina

Lechones más fuertes y numerosos al destete

El arte de alimentar a cerdas reproductoras: inteligencia artificial al servicio de la nutrición y productividad
Gustavo Márquez Esteban Pablo Fuentes Pardo Sara Crespo Vicente
Respuesta de emergencia en accidentes con transporte porcino: la experiencia danesa
Cecilie Kobek-Kjeldager Kirstin Dahl-Pedersen Mette S. Herskin
La apuesta ganadora de Porgaor, Grupo LANKA: el sistema de alimentación individualizada en maternidades, Materneo de Asserva

Gestionar la incertidumbre cuando el miedo entra en la granja
Laura Pérez Sala
Bioseguridad y control: estrategias para afrontar el PRRS y PPA en un escenario de riesgo

Cómo cuidar la salud respiratoria de los cerdos: medidas clave
Alejandro Cid González Ana I. Pastor Calonge César B. Gutiérrez Martín Mario Delgado García Óscar Mencía-Ares Sonia Martínez Martínez
MASTERFLY® BAIT: control eficaz y duradero de moscas

¿Cuáles son las medidas para el control de la cepa Rosalía de PRRS?