Las estreptococias porcinas suponen enormes pérdidas económicas en el sector, ya que son la segunda causa de mortalidad en transiciones, después de las diarreas posdestete.

Las estreptococias porcinas constituyen un gran riesgo para el bienestar animal. Streptococcus suis (S. suis) participa activamente como agente primario causando meningitis, cojeras y muertes súbitas, así como infecciones del tracto génito-urinario y mamario. Como agente secundario complica las necrosis de orejas y colas y produce neumonías tromboembólicas. Además, suponen enormes pérdidas económicas en el sector, ya que son la segunda causa de mortalidad en transiciones, después de las diarreas posdestete.
| Streptococcus suis es considerado uno de los patógenos porcinos bacterianos más importantes a nivel mundial. |

S. suis es una bacteria cocoide, grampositiva, agrupada en parejas o cadenas cortas, muy heterogénea desde el punto de vista genotípico y fenotípico. Presenta una elevada diversidad a nivel mundial, nacional, regional, local y dentro de una misma granja.

| Los antígenos capsulares permiten identificar hasta 35 serotipos, aunque actualmente esta clasificación está en revisión. El serotipo 2 es el que se aísla con mayor frecuencia en el mundo y el que produce más cuadros de meningitis, tanto en cerdos como en humanos. En España, los serotipos más frecuentes son 9 (67,4 %), 2 (14,8 %), 7 (6 %) y 8 (4 %). |
El serotipo 3 está más asociado a patologías respiratorias, en tanto que los serotipos 9 y 7 se asocian con cuadros sistémicos y meningitis.
| S. suis es un exitoso colonizador del tracto respiratorio superior de los cerdos. La invasión de las tonsilas, intestino y vías respiratorias es muy temprana tras el parto debido a la transmisión intravaginal de la madre al lechón. El 100% de los lechones son colonizados. |


La cerda pasa anticuerpos vía calostro a los lechones, que, aunque no evitan la colonización temprana de las mucosas del lechón lactante, reducen en frecuencia e intensidad las manifestaciones clínicas en lactación.
Después del destete, coincidiendo con la desaparición de los anticuerpos circulantes, las manifestaciones clínicas son más frecuentes y relevantes, en especial desde las 2-3 semanas posdestete hasta las 16 semanas de edad.

Las situaciones de estrés ambiental, como son las altas densidades, producción continua, patologías asociadas al destete y falta de ventilación, complican aún más el cuadro.
|
Es creciente el interés por la vía digestiva del S. suis, frecuente y documentada en humanos, que en el caso del cerdo se explicaría mediante dos hipótesis de infección/ transmisión al destete:
|
Tras romper las barreras mucosas (respiratorias, intestinales) o cutáneas, S. suis invade diferentes órganos y tejidos por diseminación hematógena y/o linfática, produciendo meningitis, artritis u otras patologías sistémicas (como shock séptico con muerte, poliserositis y endocarditis).

Hasta ahora, estas patologías estaban bajo control con el uso preventivo de β-lactámicos. La reducción del uso de antimicrobianos propiciada por la Unión Europea como medida necesaria para evitar resistencias, junto con la irrupción de cepas de patogenicidad atípica de PRRSv, han complicado su control, que pasa por implementar una serie de mejoras en higiene, manejo y bioseguridad que ayuden a reducir los factores predisponentes:
1. Control de patógenos claves: PRRS y SIV.
2. Bioseguridad: sistema de gestión McRebel.
3. Limpieza enérgica que permita eliminar el biofilm para lograr una correcta desinfección.
4. Manejo y control ambiental en salas de parto y transiciones.
5. Otras medidas preventivas: autovacunas específicas y mejoras en la salud digestiva mediante el control de la microbiota e integridad intestinal.

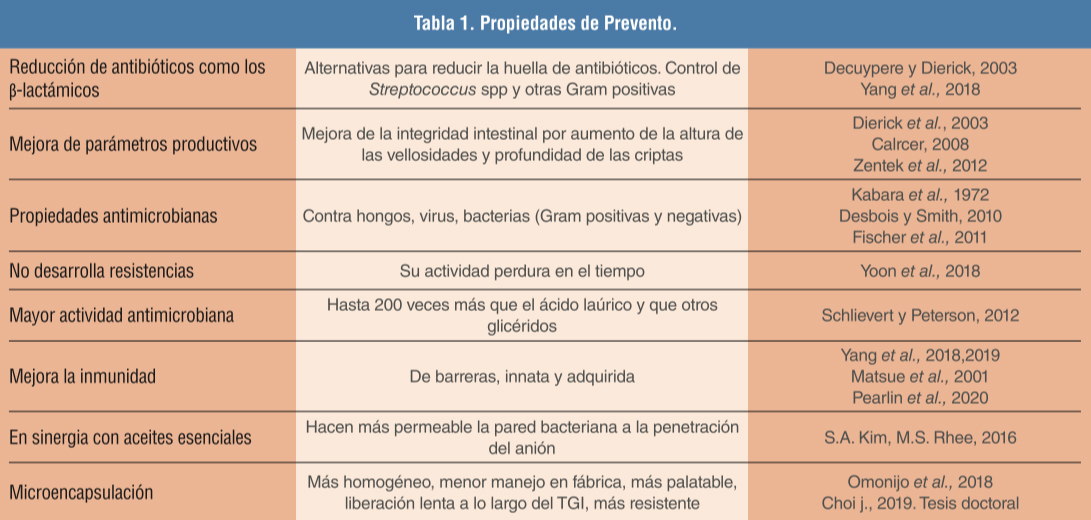
Los ácidos grasos de cadena media (AGCM) y derivados presentan tres efectos antimicrobianos:



| Por otra parte, los AGCM mejoran tanto la inmunidad de barreras (por su efecto beneficioso sobre la microbiota nasal e intestinal), como la inmunidad innata y adquirida. |
Entre los AGCM, los más eficaces en la prevención de S. suis son el ácido láurico y sus derivados esterificados.
La α-monolaurina tiene una acción contra Gram positivas muy superior a la del propio ácido láurico, así como a la de los di y triglicéridos.

En cuanto a la respuesta inmunitaria innata, la α-monolaurina tiene la capacidad de interferir en la acumulación de macrófagos productores de citocinas, sustancias que inducen a los hepatocitos a la producción de proteínas de fase aguda.
Además, la α-monolaurina puede acumularse en el calostro de las cerdas, incrementando el nivel de principio activo suministrado a los lechones a través de la leche materna, de ahí que su uso resulte muy beneficioso en la reducción de la presión de infección en salas de parto.
La microencapsulación de la α-monolaurina en matriz vegetal de liberación lenta, con inclusión de aceites esenciales que potencian sus efectos, nos permite, además, alcanzar objetivos tangibles como:




Prevento es un suplemento nutricional compuesto por éster de α-monolaurina y aceites esenciales que se presenta como una alternativa eficaz a los β-lactámicos.

El objetivo de los trabajos que se exponen fue investigar el efecto de Prevento como alternativa eficaz a la utilización de β-lactámicos, para prevenir las patologías provocadas por S. suis en lechones destetados.

El suplemento fue administrado entre junio de 2021 y diciembre de 2022 en un total de 36.474 lechones PRRSv negativos. El tratamiento consistió en la inclusión de Prevento:


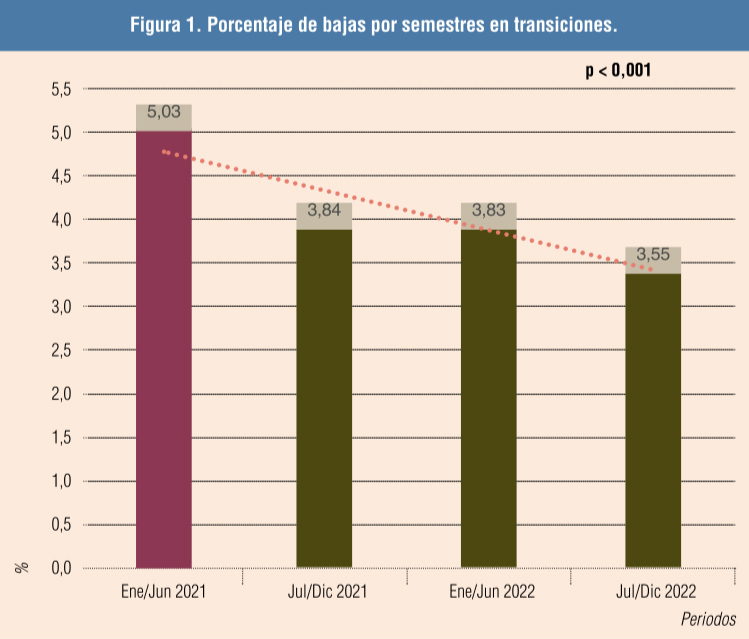
Se registraron los porcentajes de bajas sobre destetados durante los 4 semestres que duró el estudio y se compararon los datos del primer semestre de 2021 (11.490 lechones, grupo control) con los del periodo de tratamiento (julio de 2021 a diciembre de 2022).

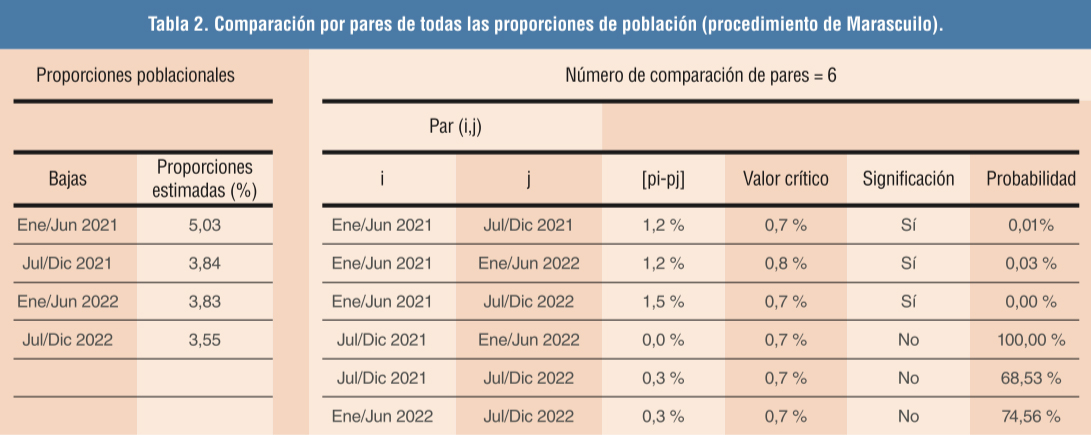
Desde la administración de la suplementación nutricional existe una significativa reducción del porcentaje de bajas posdestete sobre lechones entrados, del 5,0 al 3,5 % (p < 0,001), mantenida en el tiempo (Figura 1 y Tabla 2).

El tratamiento consistió en la inclusión en el pienso de Prevento:



Se compararon los consumos de β-lactámicos (mg/PCU), los costes de tratamiento y los datos productivos (GMD e IC) entre ambos grupos.
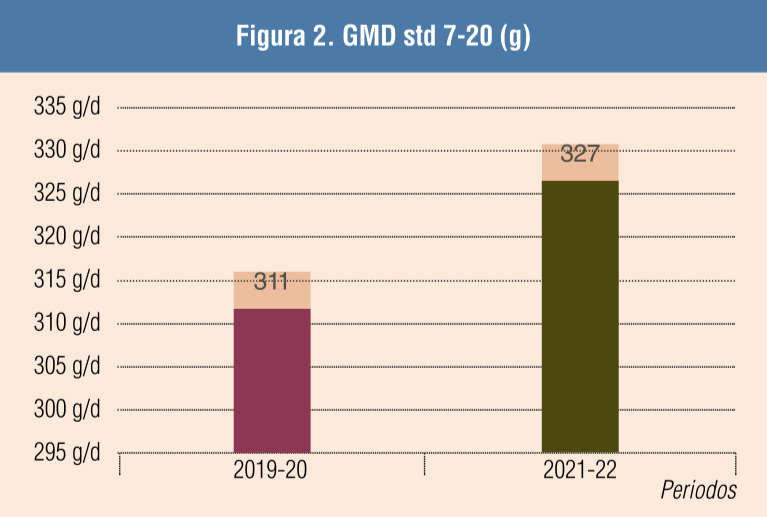
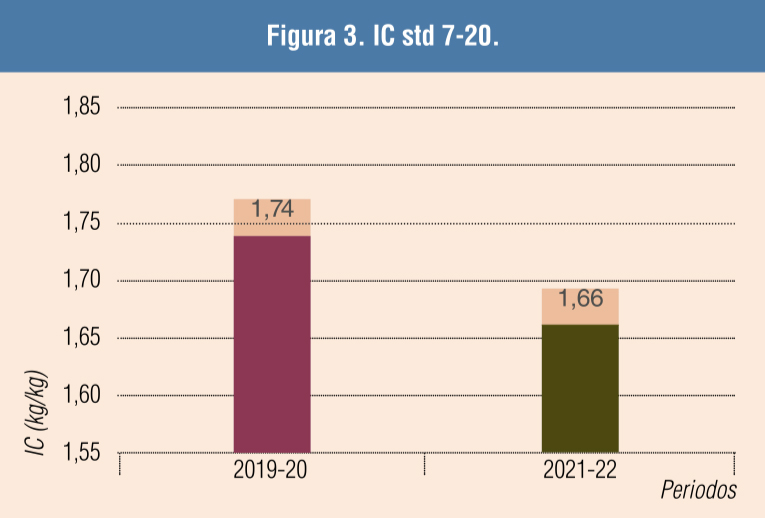
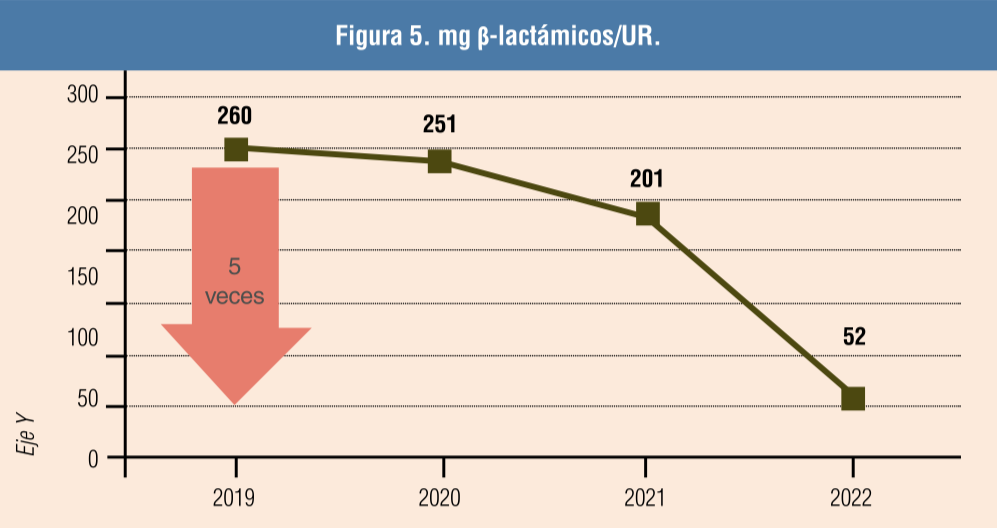
El uso del suplemento nutricional disminuyó el consumo medio de β-lactámicos hasta 5 veces (de 250 a 52 mg/PCU) en el segundo año de su uso. Se observó una ligera mejora de la GMD (16 g) y en IC (-80) en transiciones, así como una mejora sustancial en la GMD durante la fase de cebo (Figuras 2, 3, 4 y 5).
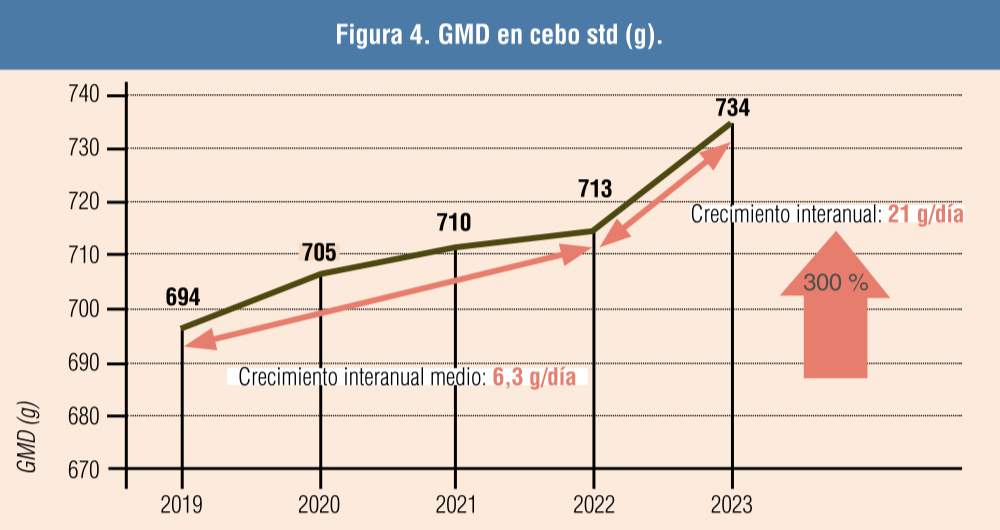
Datos propios de Porcisan referidos a Q1, Q2 y Q3 de cada año.
DATOS ECONÓMICOS
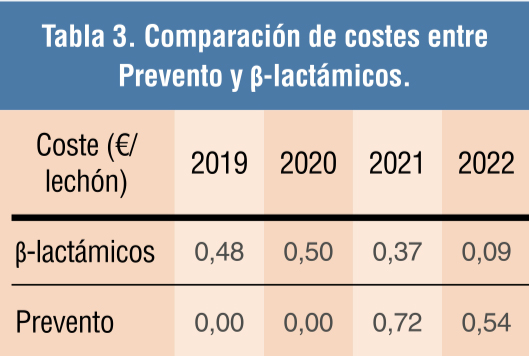
A partir del segundo año, el coste de Prevento fue similar al de β-lactámicos en años anteriores (Tabla 3 ).
|
El uso de Prevento ha demostrado ser una herramienta útil para reducir las bajas en posdestete, así como el uso de β-lactámicos. La necesidad de reducir al 50 % el consumo de antimicrobianos en producción animal entre 2020 y 2030 posiciona el uso estratégico de Prevento como una alternativa eficaz y rentable para mantener los estándares de producción. |
hoi, J. Y. 2019. Lipid matrix microencapsulation for effective delivery of essential oils and organic acids to improve gut health in weaned piglets. Tesis
Correa-Fiz et al., 2020. Aditivos alimentarios para el control de la enfermedad posdestete por Streptococ- cus suis y su efecto sobre la microbiota fecal y nasal De Snoeck, S. Ácido Laúrico y glicerol monolaurato: aditivos de futuro. Nutrinews, junio 2016.
Gottschalk, M., Segura, M. Streptococcosis. Ch. 61. Diseases of swine. 11th edition.
Goyette-Desjardins et al., 2104. Streptococcus suis, an important pig pathogen and emerging zoonotic agent—an update on the worldwide distribution based on serotyping and sequence typing
Jackman et al., 2020. Medium-chain fatty acids and monoglycerides as feed additives for pig production: towards gut health improvement and feed pathogen mitigation. Journal of Animal Science and Biotechno- logy.
Neila-Ibáñez et al., 2021. Stochastic Assessment of the Economic Impact of S suis-Associated Disease in German, Dutch and Spanish Swine Farms. Front. Vet. Sci., 19
Pérez Fernández, E. Alternativas y reducción del uso de antibióticos en el ganado porcino. Tesis Doctoral. Univ. de León 2022.
Segura, M. (2020). Streptococcus suis Research: Pro- gress and Challenges. Pathogens, 9(9), 707. MDPI AG Schlievert, P. M., Peterson M. L. Glycerol Monolau- rate Antibacterial Activity in Broth and Biofilm Cul- tures. July 2012. https://doi.org/10.1371/journal. pone.0040350.
Ver más sobre Ingaso Farm
Suscribete ahora a la revista técnica porcina
AUTORES
Necropsia – Pieza indispensable en el diagnóstico de patologías porcinas
Ronaldo Gottardo
Micotoxinas – Una amenaza invisible para la salud y productividad porcina
Panagiotis Tassis
Estrés por calor y alimentación de reproductores
Laura Batista
Streptococcus suis: Diagnóstico, serotipos más frecuentes y evolución de la sensibilidad antibiótica
Desirée Martín Jurado Mireya Melero Pérez Silvia del Caso
Microalgas, una nueva oportunidad
Braulio de la Calle Campos
Prebióticos, microbiota y salud intestinal del lechón
Alberto Morillo Alujas
Decálogo para tener lechones de calidad, una aproximación de campo – Parte II
Andrea Martínez Martínez Elena Goyena Salgado Emilio José Ruiz Fernández José Manuel Pinto Carrasco Manuel Toledo Castillo Rocío García Espejo Simón García Legaz
Concentración de dosis seminales y su influencia en la eficiencia reproductiva en granja
Álvaro Guerrero Masegosa Anselmo Martínez Moreno Henar González Ramiro Jonatan Sánchez-Osorio Juan Conesa Navarro Mª José Martínez Paula Sánchez Giménez Raquel Fernández Rodríguez
Productividad al compás de los ritmos biológicos porcinos
Guillermo Ramis Vidal
Optimizando el ambiente en granjas porcinas de engorde

Ascaris suum: un parásito subestimado con impacto económico significativo en la producción porcina en España
Descifrando la Ileítis Porcina

Lechones destetados robustos: forjando el camino hacia una salud de hierro
Dr. Christof Rapp
¿Cómo maximizar el control de la diarrea neonatal en las granjas porcinas?
Carlos Casanovas Granell David Espigares Laura Garza Salvador Oliver Sonia Cárceles Susana Mesonero Escuredo
Operación supervivencia neonatal en sistemas de parideras alternativas
Emma Baxter
Polifenoles naturales como estrategia complementaria a medidas sanitarias y de manejo frente al estrés oxidativo asociado a una cepa altamente virulenta de PRRSV en lechones
Jordi Falgueras Verdaguer Marta Bruguera Bonfill