Sin lugar a dudas, el patotipo enterotoxigénico de E. coli o ETEC es el principal patógeno involucrado, aunque otros agentes también pueden jugar un importante papel en esta etiología, actuando bien solos, combinados entre sí o con E. coli.
El destete supone un importante reto para las explotaciones porcinas, ya que existen numerosos factores que favorecen el desarrollo de cuadros diarreicos en lechones.

Las particulares condiciones que concurren en este periodo y que incluyen estrés, cambio drástico de dieta, enlentecimiento del tránsito digestivo o supresión de la inmunidad pasiva procedente de la cerda, unidas a un animal muy joven, con un sistema inmunitario aún inmaduro y con una microbiota en evolución, favorecen la aparición de cuadros de diarrea.
Además de los factores mencionados, en la etiología de las diarreas postdetete participan diferentes microorganismos patógenos.
Sin lugar a dudas, el patotipo enterotoxigénico de E. coli o ETEC es el principal patógeno involucrado, aunque otros agentes también pueden jugar un importante papel en esta etiología, actuando bien solos, combinados entre sí o con E. coli.
Entre ellos, destacan los Rotavirus y los Coronavirus y, dentro de estos últimos, en nuestro ámbito, el virus de la diarrea epidémica porcina o VDEP.
Los mecanismos de acción de estos microorganismos patógenos son diferentes y, además, tanto E. coli como Rotavirus y Coronavirus se multiplican y ejercen su acción patógena en el intestino delgado, yeyuno e íleon.
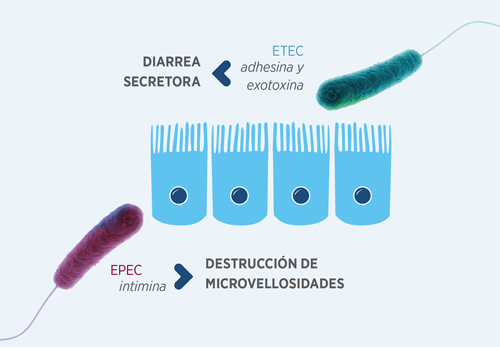
Las diarreas postdestete asociadas a E. coli son consecuencia de la presencia de factores de virulencia en los aislados patógenos de esta bacteria.
Los aislados de ETEC disponen de fimbrias u otras adhesinas que les permiten adherirse a los enterocitos y multiplicarse de forma ventajosa, así como de exotoxinas que inducen cambios en la permeabilidad de la membrana del enterocito y causan una diarrea secretora.
Con menor relevancia, se ha propuesto que también pueden participar en la etiología de las diarreas postdestete aislados de E.coli enteropatógeno o EPEC que disponen de una proteína externa de membrana, la intimina, que permite una fuerte adhesión a los enterocitos y compromete las funciones del citoesqueleto, generando lesiones de destrucción de las microvellosidades.
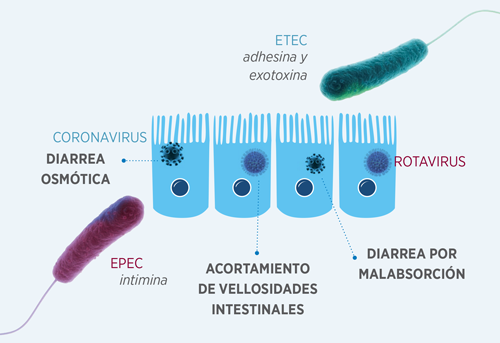
Por su parte, tanto los Rotavirus como los Coronavirus se multiplican en el citoplasma de los enterocitos maduros de las vellosidades intestinales y producen degeneración, lisis y descamación de estas células. Esto conduce a un acortamiento más o menos severo de las vellosidades intestinales y a un cuadro de diarrea por malabsorción que se complica con una diarrea osmótica asociada a la presencia de alimento no digerido en el lumen intestinal.
La gravedad de las lesiones es mayor en el caso de los Coronavirus aunque en la patogenia de las diarreas asociadas a Rotavirus también podrían participar otros mecanismos.
Se ha propuesto que la glucoproteína NSP4, producida en la replicación de los Rotavirus es una enterotoxina que altera la permeabilidad del enterocito y podría participar en la inducción del cuadro clínico de diarrea.
La disparidad en los mecanismos patogénicos permite que los efectos de estos patógenos sean, cuanto menos, aditivos.
Diferentes estudios han demostrado que la infección simultánea con virus entéricos, tanto Coronavirus como Rotavirus, agrava el cuadro clínico de diarrea en los lechones infectados con ETEC.
En este sentido, se ha propuesto que las infecciones víricas favorecen la colonización y adherencia de bacterias a nivel intestinal mediante diferentes mecanismos:

El diagnóstico de las diarreas postdestete debe ser detallado e incluir tanto a ETEC como a Rotavirus y Coronavirus.
CORONAVIRUS
La detección simultánea de ETEC y de Coronavirus en una explotación requiere de la aplicación de herramientas de control específicas para ambos agentes.
ROTAVIRUS
En el caso de los Rotavirus, el cuadro clínico asociado suele ser más leve y la interpretación de los resultados del diagnóstico etiológico es más compleja.
 No puede basarse exclusivamente en la detección de estos virus, siendo recomendable completar este diagnóstico con informes histopatológicos que permitan valorar la existencia de lesiones compatibles.
No puede basarse exclusivamente en la detección de estos virus, siendo recomendable completar este diagnóstico con informes histopatológicos que permitan valorar la existencia de lesiones compatibles.
Bibliografía
Benfield, D.A., Francis, D.H., McAdaragh, J.P., Johnson, D.D., Bergeland, M.E., Rossow, K., Moore, R., 1988. Combined rotavirus and K99 Escherichia coli infection in gnotobiotic pigs. Am. J. Vet. Res., 49 (3): 330-7.
Luppi, 2017. Swine enteric colibacillosis: diagnosis, therapy and antimicrobial resistance. Porcine Health Management, 3: 16. doi: 10.1186/s40813-017-0063-4.
Neog, B.K., Barman, N.N., Bora, D.P., Dey, S.C., Chakraborty, A., 2011. Experimental infection of pigs with group A rotavirus and enterotoxigenic Escherichia coli in India: gross, histopathological and immunopathological study. Vet. Ital. 47 (2): 117-28.
Xia, L., Dai, L., Yu, Q., Yang, Q., 2017. Persistent Transmissible Gastroenteritis Virus Infection Enhances Enterotoxigenic Escherichia coli K88 Adhesion by Promoting Epithelial-Mesenchymal Transition in Intestinal Epithelial Cells. J. Virol., 91 (21). doi: 10.1128/JVI.01256-17.
ESSWICLP00079
Suscribete ahora a la revista técnica porcina
AUTORES

El destete como punto clave de la productividad: puntos críticos a tener en cuenta
Anabel Fernández Bravo Andrea Martínez Martínez Elena Goyena Salgado Emilio José Ruiz Fernández Francisco Frances Diaz José Manuel Pinto Carrasco Manuel Toledo Castillo Simón García Legaz
2026: consolidar fortalezas para avanzar con firmeza

Energía neta y crecimiento porcino: claves para una mejor predicción
Gabriela Martínez
Estrategia nutricional active feeding en lechones destetados PRRS positivos
Alberto Morillo Alujas
Bioseguridad aplicada frente a peste porcina africana: protocolos clave en granja, logística y control externo
David García Páez
Microbiota intestinal en el cerdo: función en producción porcina

Lechones más fuertes y numerosos al destete

El arte de alimentar a cerdas reproductoras: inteligencia artificial al servicio de la nutrición y productividad
Gustavo Márquez Esteban Pablo Fuentes Pardo Sara Crespo Vicente
Respuesta de emergencia en accidentes con transporte porcino: la experiencia danesa
Cecilie Kobek-Kjeldager Kirstin Dahl-Pedersen Mette S. Herskin
La apuesta ganadora de Porgaor, Grupo LANKA: el sistema de alimentación individualizada en maternidades, Materneo de Asserva

Gestionar la incertidumbre cuando el miedo entra en la granja
Laura Pérez Sala
Bioseguridad y control: estrategias para afrontar el PRRS y PPA en un escenario de riesgo

Cómo cuidar la salud respiratoria de los cerdos: medidas clave
Alejandro Cid González Ana I. Pastor Calonge César B. Gutiérrez Martín Mario Delgado García Óscar Mencía-Ares Sonia Martínez Martínez
MASTERFLY® BAIT: control eficaz y duradero de moscas

¿Cuáles son las medidas para el control de la cepa Rosalía de PRRS?