A nivel productivo, la principal consecuencia de la inflamación intestinal es la pérdida de crecimiento. Estos procesos consumen hasta un 30% de la energía y proteína ingeridas, afectando al índice de conversión.
La inflamación intestinal, además de afectar al bienestar animal, afecta negativamente a la conversión alimentaria, siendo recomendable adoptar estrategias nutricionales con efectos antiinflamatorios que favorezcan la salud intestinal.

![]() LA SALUD INTESTINAL
LA SALUD INTESTINAL
La reducción de antibióticos para procesos digestivos requiere tener en cuenta cuáles son los componentes de algo tan complejo y difícil de definir como la salud intestinal. Una posible definición de salud intestinal sería: “un estado estable donde el microbioma y el tracto intestinal existen en equilibrio simbiótico y donde el bienestar y el rendimiento del animal no están limitados por una disfunción intestinal” (Bischoff, 2011).
Esta definición combina los tres componentes principales de la salud intestinal (dieta, mucosa intestinal y microbiota) con una digestión y absorción de nutrientes eficaz y un estado inmune efectivo.
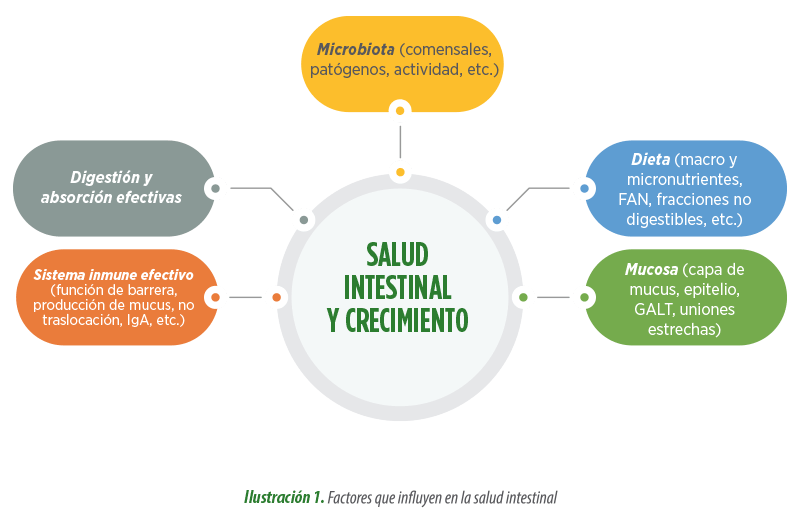
Centrándonos en la mucosa intestinal, cabe destacar de entre sus funciones, el papel que ejerce como barrera intestinal con diferentes acciones al respecto:



La expresión de los factores de barrera intestinal está controlada en gran parte por el reconocimiento de la microbiota por parte del sistema inmune innato y previniendo una respuesta inmune exagerada.
 LA INFLAMACIÓN INTESTINAL
LA INFLAMACIÓN INTESTINAL
Una perturbación de la homeostasis entre dieta – barrera intestinal – microbiota puede provocar:




La inflamación es una respuesta fisiológica cuando existe daño en un tejido debido a causas físicas (heridas, cuerpos extraños, radiación, calor, etc.) o biológicas (virus, bacterias, hongos, etc.). El objetivo de la inflamación es eliminar la causa, prevenir la expansión del daño y restaurar la funcionalidad del tejido dañado.

![]() LOS EFECTOS MÁS IMPORTANTES DE LA INFLAMACIÓN A NIVEL INTESTINAL SON
LOS EFECTOS MÁS IMPORTANTES DE LA INFLAMACIÓN A NIVEL INTESTINAL SON





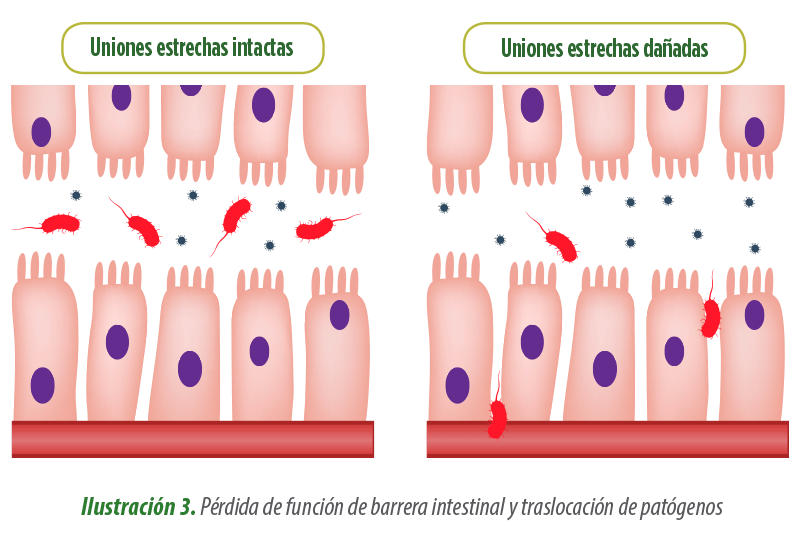
La hiperpermeabilidad intestinal contribuye en la patogénesis de muchas patologías del tracto gastrointestinal. Una barrera intestinal perturbada se caracteriza por un mayor número de receptores TLR-4 (excesiva activación del sistema inmune) y promueve la fuga de antígenos al torrente sanguíneo.
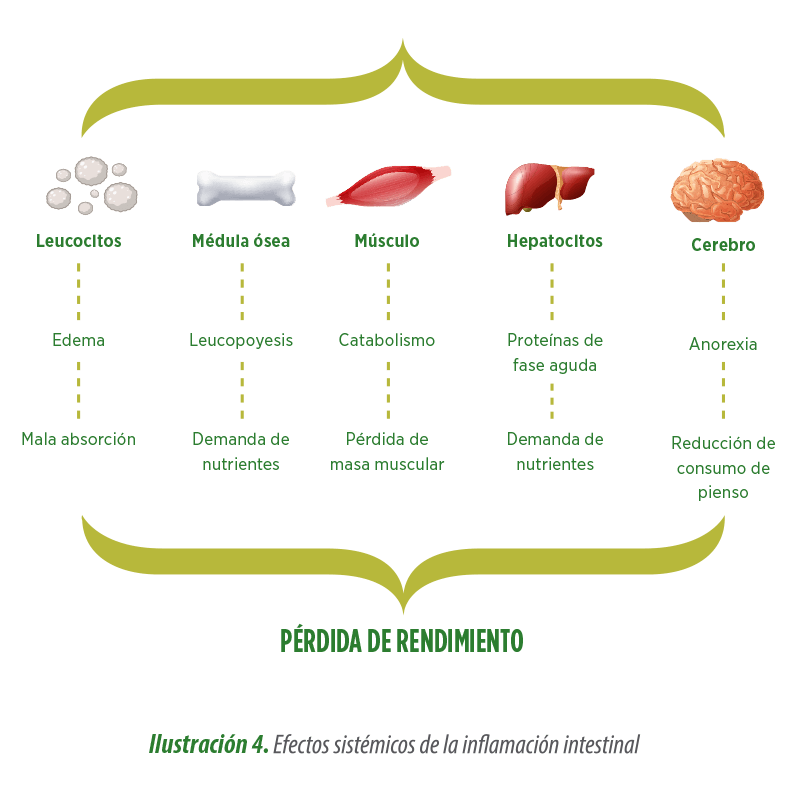
Como resultado final del proceso inflamatorio intestinal se producen efectos tanto a nivel local como sistémico: Inflamación intestinal







 ¿CUÁNDO SE PRODUCE LA INFLAMACIÓN INTESTINAL?
¿CUÁNDO SE PRODUCE LA INFLAMACIÓN INTESTINAL?
Un tracto gastrointestinal sano está en un estado constante de inflamación “controlada”, como consecuencia de la presencia de una elevada población de bacterias, antígenos dietéticos y toxinas.
Este estado de inflamación controlada permite una activación basal del sistema inmunitario del TGI, que asociado con una microbiota comensal “normal”, tiene efectos positivos en el mantenimiento de la funcionalidad intestinal y la capacidad de digerir y absorber los nutrientes de los cerdos.
![]() SON VARIAS LAS POSIBLES CAUSAS DE INFLAMACIÓN. ALGUNAS DE LAS MÁS IMPORTANTES:
SON VARIAS LAS POSIBLES CAUSAS DE INFLAMACIÓN. ALGUNAS DE LAS MÁS IMPORTANTES:





A nivel productivo, la principal consecuencia de la inflamación intestinal es la pérdida de crecimiento. Estos procesos consumen hasta un 30% de la energía y proteína ingeridas, afectando al índice de conversión.

 ¿CÓMO REGULAR LA INFLAMACIÓN INTESTINAL?
¿CÓMO REGULAR LA INFLAMACIÓN INTESTINAL?
EFECTOS DE LOS ALCALOIDES ISOQUINOLÍNICOS
En los últimos años, varios estudios han demostrado la actividad antiinflamatoria de los antibióticos promotores del crecimiento como responsable de parte de su efecto. Esta mejora de la función de barrera intestinal se asocia a una expresión reducida de citoquinas proinflamatorias.
Existe un nuevo enfoque nutricional para reducir los efectos de la inflamación intestinal, como puede ser, por ejemplo, el uso de algunos componentes vegetales específicos.
El efecto primario de estos alcaloides es el bloqueo del receptor NF-κB, que es el factor de transcripción clave para el desarrollo de la cascada de señales pro-inflamatorias en el intestino. La activación de este receptor induce la síntesis de ciclooxigenasa, fosfolipasa A2, iNOS, citoquinas, etc. Por tanto, la inflamación intestinal local acaba teniendo también un efecto a nivel sistémico.
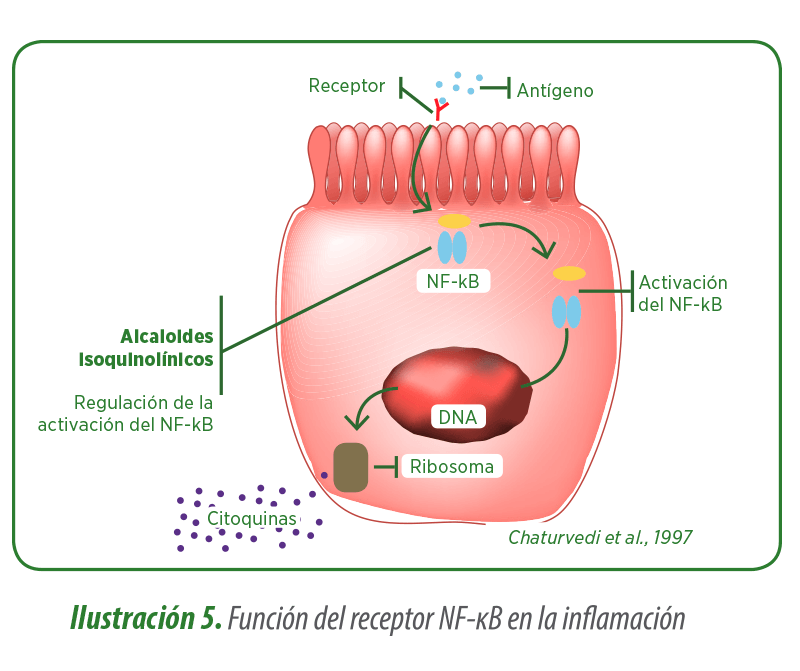
 Gracias al bloqueo de este receptor, los alcaloides isoquinolínicos actúan antes de la síntesis de factores pro-inflamatorios, reduciendo así el coste de la inflamación a nivel sistémico (protección hepática, antioxidante) y a nivel productivo, siendo sus efectos dosis-dependiente. Al mismo tiempo, permiten el nivel de inflamación basal necesario para una inmunidad eficiente en el intestino (efecto dosis-dependiente).
Gracias al bloqueo de este receptor, los alcaloides isoquinolínicos actúan antes de la síntesis de factores pro-inflamatorios, reduciendo así el coste de la inflamación a nivel sistémico (protección hepática, antioxidante) y a nivel productivo, siendo sus efectos dosis-dependiente. Al mismo tiempo, permiten el nivel de inflamación basal necesario para una inmunidad eficiente en el intestino (efecto dosis-dependiente).
Los efectos derivados del uso de componentes vegetales específicos se podrían resumir en:
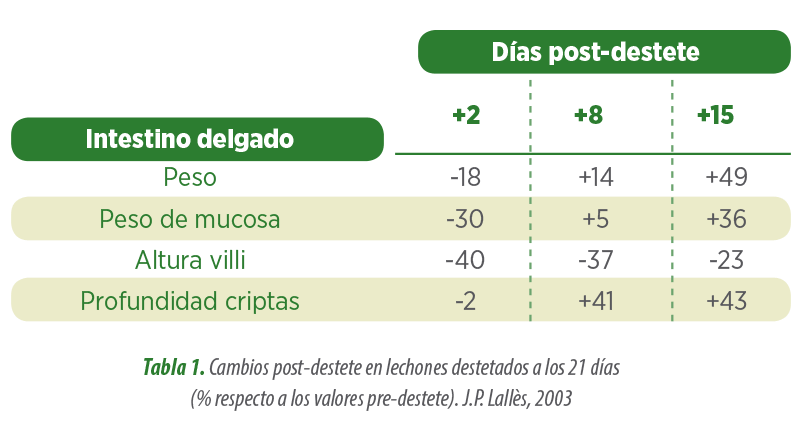
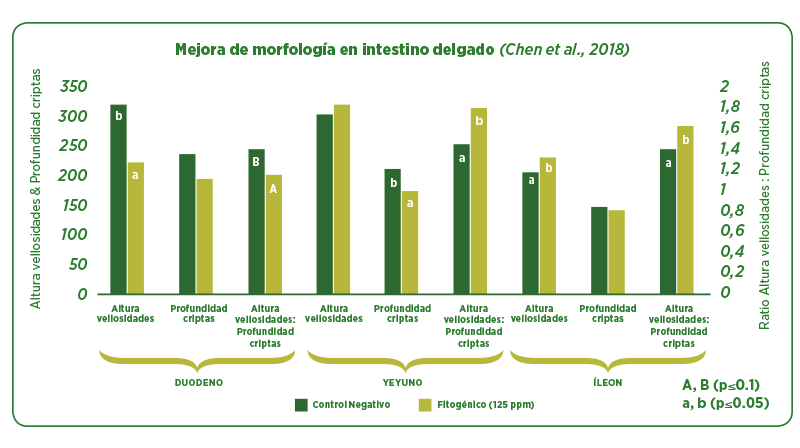
En el ensayo realizado por Chen et al. (2018), se estudió el efecto de la inclusión de un fitogénico rico en alcaloides isoquinolínicos sobre la morfología intestinal de lechones destetados a 21 días de vida durante las primeras semanas post-destete.
Los resultados obtenidos fueron:





Existen otras estrategias dirigidas a bloquear este receptor y controlar la inflamación intestinal (curcumina, antioxidantes, corticosteroides, etc.) pero sin relevancia práctica en la producción porcina. Otros productos con efecto antiinflamatorio actúan una vez iniciada la cascada inflamatoria, por lo que no reducen todos los efectos a nivel sistémico.
EN EL MANEJO DE LA SALUD INTESTINAL SIN ANTIBIÓTICOS DEBEMOS RECORDAR QUE:





Suscribete ahora a la revista técnica porcina
AUTORES

Bioseguridad aplicada frente a Peste Porcina Africana: protocolos clave en granja, logística y control externo
David García Páez
Cómo cuidar la salud respiratoria de los cerdos: medidas clave
Alejandro Cid González Ana I. Pastor Calonge César B. Gutiérrez Martín Mario Delgado García Óscar Mencía-Ares Sonia Martínez Martínez
2026: consolidar fortalezas para avanzar con firmeza

Respuesta de emergencia en accidentes con transporte porcino: la experiencia danesa
Cecilie Kobek-Kjeldager Kirstin Dahl-Pedersen Mette S. Herskin
Microbiota intestinal en el cerdo: de la taxonomía a la función en producción porcina
Eduard de la Torre Candán
Energía neta y crecimiento porcino: claves para una mejor predicción
Gabriela Martínez
La apuesta ganadora de Porgaor, Grupo LANKA: el sistema de alimentación individualizada en maternidades, Materneo de Asserva

El arte de alimentar a cerdas reproductoras: inteligencia artificial al servicio de la nutrición y productividad
Gustavo Márquez Esteban Pablo Fuentes Pardo Sara Crespo Vicente
Lechones más fuertes y numerosos al destete

Estrategia nutricional active feeding en lechones destetados PRRS positivos
Alberto Morillo Alujas
MASTERFLY® BAIT: control eficaz y duradero de moscas

El destete como punto clave de la productividad: puntos críticos a tener en cuenta
Anabel Fernández Bravo Andrea Martínez Martínez Elena Goyena Salgado Emilio José Ruiz Fernández Francisco Frances Diaz José Manuel Pinto Carrasco Manuel Toledo Castillo Simón García Legaz
Medidas para el control de la cepa Rosalía de PRRS

Gestionar la incertidumbre cuando el miedo entra en la granja
Laura Pérez Sala
Bioseguridad y control: estrategias para afrontar el PRRS y PPA en un escenario de riesgo