Artículo adaptado de: Jacobs AAC, et al. Efficacy of a novel inactivated Lawsonia intracellularis vaccine in pigs against experimental infection and under field conditions. Vaccine. doi: 10.1016/j.vaccine.2019.02.067
Recientemente se ha presentado una nueva vacuna inactivada frente a L. intracellularis, Porcilis® Lawsonia, que es combinable con Porcilis® PCV M Hyo.

Artículo adaptado de: Jacobs AAC, et al. Efficacy of a novel inactivated Lawsonia intracellularis vaccine in pigs against experimental infection and under field conditions. Vaccine. doi: 10.1016/j.vaccine.2019.02.067
INTRODUCCIÓN
La enteritis proliferativa porcina, también conocida como ileítis, es una enfermedad infecciosa intestinal caracterizada por el engrosamiento de la mucosa intestinal del tramo distal del intestino delgado y del proximal del intestino grueso, como resultado de la proliferación de enterocitos asociada a la presencia de la bacteria intracelular Lawsonia intracellularis1.
 Este patógeno intestinal porcino ha sido identificado como uno de los principales patógenos entéricos en cerdos de cebo a nivel mundial, con una prevalencia de entre el 48 y el 100% en los países productores de cerdos2–4.
Este patógeno intestinal porcino ha sido identificado como uno de los principales patógenos entéricos en cerdos de cebo a nivel mundial, con una prevalencia de entre el 48 y el 100% en los países productores de cerdos2–4.
Recientemente, se ha desarrollado una vacuna inactivada segura y eficaz frente a L. intracellularis, Porcilis® Lawsonia, que es combinable con Porcilis® PCV M Hyo.
Esta nueva vacuna inactivada consiste en una fracción de antígeno liofilizada y una fracción soluble que contiene el adyuvante.
Esta fracción de antígeno liofilizada para L. intracellularis se reconstituye justo antes de su uso en el disolvente y se administra de forma intramuscular mediante una sola dosis de 2 ml a los lechones a partir de las 3 semanas de vida.
![]() De forma alternativa, esta fracción liofilizada se puede reconstituir con Porcilis® PCV M Hyo y ser administrada en uso mixto asociada con la vacuna bivalente.
De forma alternativa, esta fracción liofilizada se puede reconstituir con Porcilis® PCV M Hyo y ser administrada en uso mixto asociada con la vacuna bivalente.


![]()
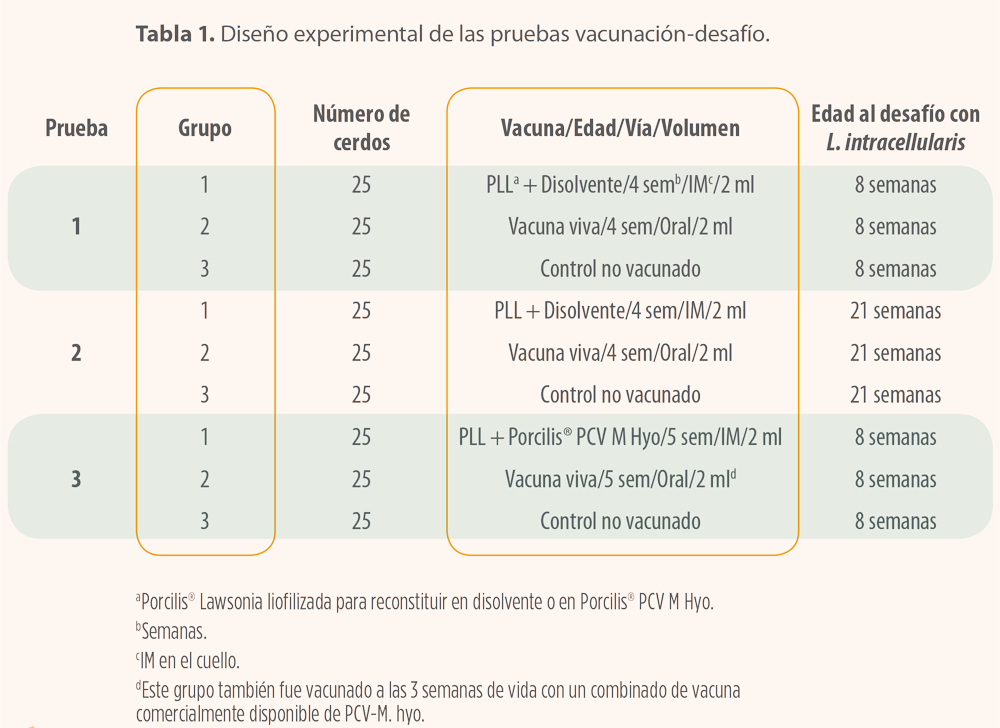
Se plantearon tres estudios con un diseño similar (tabla 1). Para cada prueba se seleccionaron 75 lechones de una granja negativa a Mycoplasma hyopneumoniae (Mhyo) y PRRSV, sin historial de infecciones por L. intracellularis, que fueron distribuidos en tres grupos de 25 lechones cada uno.
En el GRUPO 1 se vacunaron una vez por vía intramuscular con 2 ml de Porcilis® Lawsonia a las 4 semanas de vida (estudios 1 y 2) o con 2 ml de Porcilis® Lawsonia mezclada con Porcilis® PCV M Hyo a las 5 semanas de vida (estudio 3).
![]() Los lechones del GRUPO 2 se vacunaron por vía oral con 2 ml de la vacuna viva a las 4 semanas de vida (estudios 1 y 2) o a las 5 semanas de vida (estudio 3).
Los lechones del GRUPO 2 se vacunaron por vía oral con 2 ml de la vacuna viva a las 4 semanas de vida (estudios 1 y 2) o a las 5 semanas de vida (estudio 3).
![]() El último grupo, encuadrado dentro del estudio 3, recibió 2 ml de una mezcla de vacunas frente a PCV2 y M hyo a las 3 semanas de vida. En este grupo, en el caso de la vacuna viva frente a L. intracellularis, se tuvo que realizar de forma separada a las 5 semanas de vida porque no tiene registro de uso concurrente con otras vacunas.
El último grupo, encuadrado dentro del estudio 3, recibió 2 ml de una mezcla de vacunas frente a PCV2 y M hyo a las 3 semanas de vida. En este grupo, en el caso de la vacuna viva frente a L. intracellularis, se tuvo que realizar de forma separada a las 5 semanas de vida porque no tiene registro de uso concurrente con otras vacunas.
En los tres estudios, el GRUPO 3 se dejó como control no vacunado.
![]()
 Los cerdos fueron expuestos a Lawsonia intracellularis:
Los cerdos fueron expuestos a Lawsonia intracellularis:
4 semanas después de la vacunación (estudio 1),
17 semanas después de la vacunación (estudio 2) o
3 semanas después de la última vacunación (estudio 3).
 El desafío se llevó a cabo mediante la administración oral de mucosa intestinal homogeneizada infectada con L. intracellularis. Los cerdos se observaron diariamente para detectar signos clínicos de ileítis y se pesaron a intervalos semanales durante un periodo posdesafío de 21 días.
El desafío se llevó a cabo mediante la administración oral de mucosa intestinal homogeneizada infectada con L. intracellularis. Los cerdos se observaron diariamente para detectar signos clínicos de ileítis y se pesaron a intervalos semanales durante un periodo posdesafío de 21 días.
![]() Se recogieron muestras de suero el día de la vacunación, el día de la exposición y el día de la necropsia.
Se recogieron muestras de suero el día de la vacunación, el día de la exposición y el día de la necropsia.
![]() 21 días después del desafío todos los cerdos fueron sacrificados y se les realizó una necropsia.
21 días después del desafío todos los cerdos fueron sacrificados y se les realizó una necropsia.
![]() Durante la necropsia se tomaron muestras fecales del recto para analizarlas en una qPCR específica para L. intracellularis.
Durante la necropsia se tomaron muestras fecales del recto para analizarlas en una qPCR específica para L. intracellularis.
 Los intestinos, en particular el íleon, se analizaron macroscópicamente para detectar infección por Lawsonia intracellularis y se recogieron muestras de íleon para qPCR y puntuación inmunohistológica (IHC).
Los intestinos, en particular el íleon, se analizaron macroscópicamente para detectar infección por Lawsonia intracellularis y se recogieron muestras de íleon para qPCR y puntuación inmunohistológica (IHC).


El material de desafío se preparó a partir de raspados intestinales derivados de cerdos infectados por L. intracellularis (casos de campo).

 Se revisó la sintomatología clínica en todos los cerdos para detectar cualquier signo de infección por L. intracellularis justo antes del desafío y diariamente una vez desafiados.
Se revisó la sintomatología clínica en todos los cerdos para detectar cualquier signo de infección por L. intracellularis justo antes del desafío y diariamente una vez desafiados.
![]() Para clasificarlos se usó este sistema de puntuación:
Para clasificarlos se usó este sistema de puntuación:
0 = normal,
1 = diarrea leve,
2 = diarrea moderada,
3 = diarrea grave y/o con presencia de sangre;
también se describió cualquier otra anomalía.
Los animales que murieron o fueron eutanasiados debido a una infección grave por L. intracellularis se les asignó una puntuación 3 a cada uno de los puntos de observación restantes para permitir que la magnitud del efecto clínico se reconociera adecuadamente en el análisis.
![]() En este modelo los signos clínicos se hicieron evidentes la tercera semana posdesafío.
En este modelo los signos clínicos se hicieron evidentes la tercera semana posdesafío.
Las puntuaciones clínicas diarias de los 13 a los 20 días después del desafío se totalizaron y promediaron por grupo.

 Los cerdos se pesaron un día antes del desafío y los días 6, 13 y 20 posdesafío. En este modelo de desafío el efecto negativo sobre el crecimiento empezó a ser aparente a partir de la tercera semana posdesafío (días 13 a 20), semana en la cual se calculó la GMD de forma individual y también se realizó la media de cada grupo.
Los cerdos se pesaron un día antes del desafío y los días 6, 13 y 20 posdesafío. En este modelo de desafío el efecto negativo sobre el crecimiento empezó a ser aparente a partir de la tercera semana posdesafío (días 13 a 20), semana en la cual se calculó la GMD de forma individual y también se realizó la media de cada grupo.

Tres semanas después del desafío los cerdos fueron sacrificados y se realizó un examen post mortem. En la necropsia se examinaron los intestinos, en particular el íleon (los últimos 0,5 m del intestino delgado), para detectar lesiones indicativas de infección por L. intracellularis.
Se recogió una muestra fecal (del recto) y una muestra de íleon (5 cm por encima de la unión ileocecal) de cada animal para analizarlas en una qPCR específica de L. intracellularis.
Además, se recogió una muestra de íleon y se fijó en formol al 4 %, que luego se procesó en portaobjetos.
 Estos portaobjetos se tiñeron con hematoxilina-eosina (tinción HE) y con una tinción inmunohistoquímica mediante el uso de un anticuerpo monoclonal anti-L. intracellularis (tinción IHC) y se examinaron microscópicamente.
Estos portaobjetos se tiñeron con hematoxilina-eosina (tinción HE) y con una tinción inmunohistoquímica mediante el uso de un anticuerpo monoclonal anti-L. intracellularis (tinción IHC) y se examinaron microscópicamente.
![]() La mucosa del íleon se puntuó de forma macroscópica mediante este sistema de puntuación:
La mucosa del íleon se puntuó de forma macroscópica mediante este sistema de puntuación:
0 = normal;
0,5 = ligero engrosamiento;
1 = engrosamiento leve;
2 = moderado;
3 = grave engrosamiento y/o enrojecimiento;
4 = grave engrosamiento y/o enrojecimiento con presencia de fibrina y/o necrosis.
 Además, el porcentaje de íleon afectado se estimó tal y como sigue: la longitud de la parte de íleon afectada se dividió por la longitud total de íleon y el resultado se multiplicó por 100.
Además, el porcentaje de íleon afectado se estimó tal y como sigue: la longitud de la parte de íleon afectada se dividió por la longitud total de íleon y el resultado se multiplicó por 100.
La puntuación de lesiones en el total del íleon se calculó mediante la multiplicación de la puntuación de la mucosa del íleon y el porcentaje de íleon afectado. El promedio de lesiones en el total del íleon se calculó para cada grupo de tratamiento.

![]() La puntuación histológica se obtuvo mediante este sistema para HE:
La puntuación histológica se obtuvo mediante este sistema para HE:
0 = no se detectan anomalías,
0,5 = lesión dudosa,
1 = lesiones leves,
2 = lesiones moderadas,
3 = lesiones graves.
![]()
 Para la tinción IHC:
Para la tinción IHC:
0 = sin evidencia de bacterias,
0,5 = presencia dudosa de bacterias,
1 = presencia de un número bajo de bacterias en el corte,
2 = presencia de un número moderado de bacterias,
3 = presencia de un alto número de bacterias en el corte.
 La puntuación histológica total se obtuvo con la multiplicación de la puntuación HE por la de la puntuación IHC. El promedio de puntuación histológica total se calculó para cada grupo.
La puntuación histológica total se obtuvo con la multiplicación de la puntuación HE por la de la puntuación IHC. El promedio de puntuación histológica total se calculó para cada grupo.


Las muestras de suero se testaron en un ELISA interno de anticuerpos de L. intracellularis.
RESULTADOS
![]() Prueba 1
Prueba 1
El día del desafío (4 semanas después de la vacunación) el grupo 1 mostró una seroconversión activa evidente mientras que los títulos de anticuerpos en los grupos 2 y 3 se mantuvieron a un nivel comparable a la prevacunación.
Todos los grupos desarrollaron un aumento en la respuesta de anticuerpos el día de la necropsia, 3 semanas después del desafío (figura 1).
 Durante el estudio, tres animales fueron sacrificados antes del día fijado para el examen post mortem. Un animal (grupo 2) por problemas locomotores. Un segundo animal (grupo 1) por problemas neurológicos (Streptococcus suis). Un tercer animal (grupo 3) se eutanasió 20 días posdesafío debido a la enfermedad específica de L. intracellularis, es decir, varios días con diarrea, pérdida de peso y deterioro en su condición corporal.
Durante el estudio, tres animales fueron sacrificados antes del día fijado para el examen post mortem. Un animal (grupo 2) por problemas locomotores. Un segundo animal (grupo 1) por problemas neurológicos (Streptococcus suis). Un tercer animal (grupo 3) se eutanasió 20 días posdesafío debido a la enfermedad específica de L. intracellularis, es decir, varios días con diarrea, pérdida de peso y deterioro en su condición corporal.
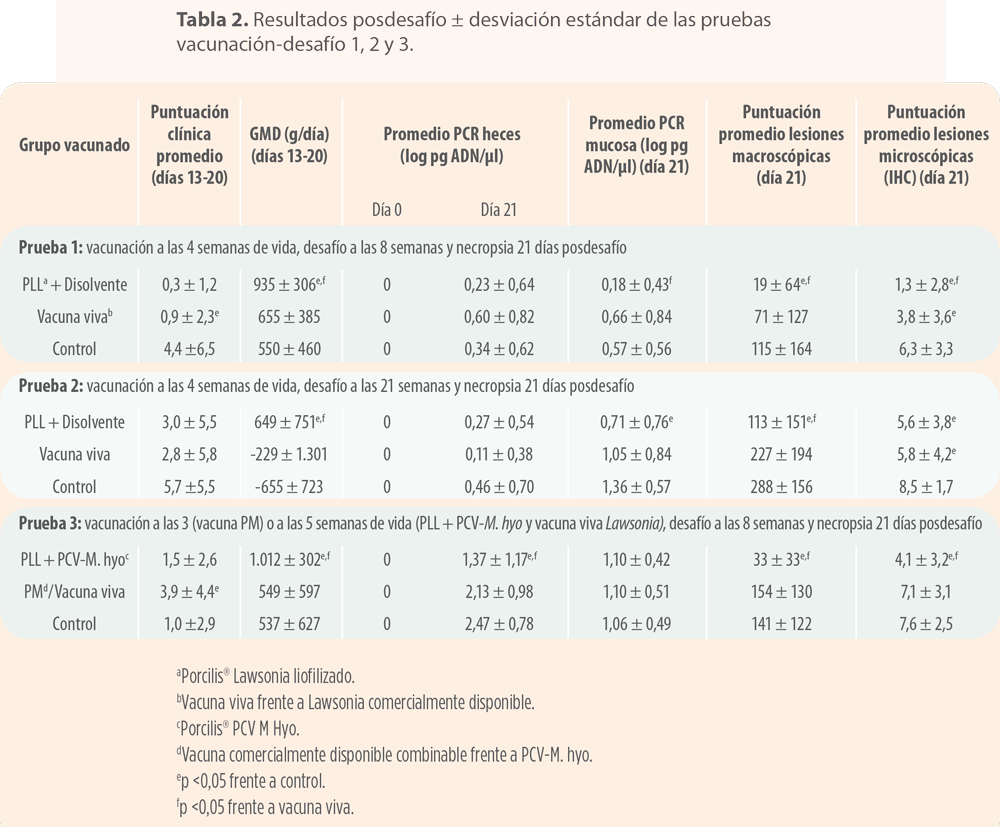
![]() En la tercera semana después del desafío los animales control habían desarrollado signos clínicos por la infección de L. intracellularis caracterizados por diarrea, una GMD subóptima y excreción de L. intracellularis en heces (tabla 2).
En la tercera semana después del desafío los animales control habían desarrollado signos clínicos por la infección de L. intracellularis caracterizados por diarrea, una GMD subóptima y excreción de L. intracellularis en heces (tabla 2).
![]() Tras la necropsia, la infección de L. intracellularis se confirmó mediante lesiones macroscópicamente visibles en el íleon, PCR positiva de la mucosa y puntuaciones de las lesiones inmunohistológicas.
Tras la necropsia, la infección de L. intracellularis se confirmó mediante lesiones macroscópicamente visibles en el íleon, PCR positiva de la mucosa y puntuaciones de las lesiones inmunohistológicas.
![]() Los cerdos vacunados con Porcilis® Lawsonia mostraron una reducción estadísticamente significativa en los signos clínicos, en la pérdida de peso (GMD de 935 g frente a 550 g) y las puntuaciones de lesiones ileales macroscópicas y microscópicas en comparación con los controles.
Los cerdos vacunados con Porcilis® Lawsonia mostraron una reducción estadísticamente significativa en los signos clínicos, en la pérdida de peso (GMD de 935 g frente a 550 g) y las puntuaciones de lesiones ileales macroscópicas y microscópicas en comparación con los controles.
![]() Además, en comparación con el grupo 2 (vacunado con vacuna oral), los siguientes parámetros mejoraron de forma significativa:
Además, en comparación con el grupo 2 (vacunado con vacuna oral), los siguientes parámetros mejoraron de forma significativa:
![]() GMD
GMD
![]() carga bacteriana en la mucosa del íleon (por PCR)
carga bacteriana en la mucosa del íleon (por PCR)
![]() puntuación de las lesiones macroscópicas
puntuación de las lesiones macroscópicas
![]() puntuación de las lesiones microscópicas
puntuación de las lesiones microscópicas
![]() Prueba 2
Prueba 2
El día del desafío (17 semanas después de la vacunación frente a L. intracellularis), los cerdos del grupo 1 mostraron una seroconversión evidente y activa, mientras que los títulos de anticuerpos medidos en los grupos 2 y 3 se mantuvieron en los niveles de antes de la vacunación.
Todos los grupos desarrollaron una mayor respuesta de anticuerpos el día de la necropsia, 3 semanas después del desafío (figura 2).
 Durante el estudio, cuatro animales fueron sacrificados antes del día fijado para el examen post mortem. Un animal (grupo 1) por problemas de locomoción. Tres animales (dos del grupo 2 y uno del grupo 3) se sacrificaron a los 17 días posdesafío debido a enfermedad específica de ileítis.
Durante el estudio, cuatro animales fueron sacrificados antes del día fijado para el examen post mortem. Un animal (grupo 1) por problemas de locomoción. Tres animales (dos del grupo 2 y uno del grupo 3) se sacrificaron a los 17 días posdesafío debido a enfermedad específica de ileítis.
En la tercera semana después del desafío los animales control habían desarrollado signos clínicos por la infección de L. intracellularis caracterizados por diarrea, pérdida de peso y excreción de L. intracellularis en heces (tabla 2).

![]() Tras la necropsia, la infección de L. intracellularis se confirmó mediante lesiones típicas macroscópicamente visibles en el íleon, PCR positiva de la mucosa y puntuaciones de las lesiones inmunohistológicas.
Tras la necropsia, la infección de L. intracellularis se confirmó mediante lesiones típicas macroscópicamente visibles en el íleon, PCR positiva de la mucosa y puntuaciones de las lesiones inmunohistológicas.
![]() Los cerdos vacunados con Porcilis® Lawsonia mostraron una reducción estadísticamente significativa en los signos clínicos, en la pérdida de peso (GMD de 649 g frente a -655 g), en la carga bacteriana en la mucosa ileal (PCR) y en las puntuaciones de lesiones ileales macroscópicas y microscópicas en comparación con los controles.
Los cerdos vacunados con Porcilis® Lawsonia mostraron una reducción estadísticamente significativa en los signos clínicos, en la pérdida de peso (GMD de 649 g frente a -655 g), en la carga bacteriana en la mucosa ileal (PCR) y en las puntuaciones de lesiones ileales macroscópicas y microscópicas en comparación con los controles.
![]() Además, en comparación con el grupo 2 (vacuna viva), los siguientes parámetros mejoraron de forma significativa:
Además, en comparación con el grupo 2 (vacuna viva), los siguientes parámetros mejoraron de forma significativa:
![]() GMD
GMD
![]() puntuación de las lesiones macroscópicas
puntuación de las lesiones macroscópicas
![]() puntuación de las lesiones microscópicas
puntuación de las lesiones microscópicas

![]() Prueba 3
Prueba 3
El día del desafío (3 semanas posvacunación), la seroconversión activa fue evidente en el grupo 1 mientras que los niveles de los grupos 2 y 3 se mantuvieron como antes de aplicar la vacuna.

Durante el estudio se tuvo que sacrificar a un animal del grupo 1 el día 7 posdesafío por problemas locomotores y un empeoramiento en su condición corporal.
La tercera semana posdesafío los animales del grupo control desarrollaron sintomatología clínica debido a la infección por L. intracellularis caracterizada por diarrea, una GMD subóptima y la excreción de L. intracellularis en heces (tabla 2).
![]() Tras la necropsia se confirmó la infección por L. intracellularis gracias a la presencia de las lesiones macroscópicas típicas en el íleon, PCR positiva en mucosa y la puntuación de las lesiones inmunohistológicas.
Tras la necropsia se confirmó la infección por L. intracellularis gracias a la presencia de las lesiones macroscópicas típicas en el íleon, PCR positiva en mucosa y la puntuación de las lesiones inmunohistológicas.
![]() Los cerdos vacunados con Porcilis® Lawsonia mostraron una reducción estadísticamente significativa en cuanto a la pérdida de peso (GMD fue de 1.012 g frente a tan solo 537 g), una menor excreción (PCR en heces) y una puntuación más baja en las lesiones microscópicas ileales, en comparación con el grupo control.
Los cerdos vacunados con Porcilis® Lawsonia mostraron una reducción estadísticamente significativa en cuanto a la pérdida de peso (GMD fue de 1.012 g frente a tan solo 537 g), una menor excreción (PCR en heces) y una puntuación más baja en las lesiones microscópicas ileales, en comparación con el grupo control.
![]() Además, estos mismos parámetros también se redujeron significativamente en comparación con el grupo 2 (vacuna viva).
Además, estos mismos parámetros también se redujeron significativamente en comparación con el grupo 2 (vacuna viva).

 En este estudio se comparó y se demostró la eficacia de una vacuna inactivada administrada por vía intramuscular frente a una vacuna viva atenuada administrada por vía oral, frente a la enfermedad digestiva causada por Lawsonia intracellularis.
En este estudio se comparó y se demostró la eficacia de una vacuna inactivada administrada por vía intramuscular frente a una vacuna viva atenuada administrada por vía oral, frente a la enfermedad digestiva causada por Lawsonia intracellularis.
Estos resultados van en línea con los publicados previamente por Roerink et al.13, que también demostraron una buena protección frente a una infección experimental por L. intracellularis mediante el uso de una vacuna inactivada de células enteras.
 Aunque se desconoce el mecanismo exacto de protección, y contrariamente al conocimiento general sobre inmunología, la vacuna inactivada conlleva una mayor protección comparada con la de una vacuna viva comercial.
Aunque se desconoce el mecanismo exacto de protección, y contrariamente al conocimiento general sobre inmunología, la vacuna inactivada conlleva una mayor protección comparada con la de una vacuna viva comercial.
El objetivo de la segunda prueba de vacunación-desafío fue comparar la duración de la inmunidad de la vacuna inactivada con la de la vacuna viva atenuada.
![]() Los resultados mostraron una afectación más grave en los animales control de los estudios 1 y 3, con una pérdida promedio de peso vivo de 655 g/día la tercera semana después del desafío.
Los resultados mostraron una afectación más grave en los animales control de los estudios 1 y 3, con una pérdida promedio de peso vivo de 655 g/día la tercera semana después del desafío.
A pesar de la gravedad del desafío, la vacuna inactivada indujo una protección robusta. La razón de las diferencias en susceptibilidad de los animales control podría estar relacionada con la edad de los animales ya que, por ejemplo, los animales de mayor edad son más susceptibles.
![]() Esto es coherente con la situación en campo donde los animales más adultos son los que se ven afectados unas semanas antes del sacrificio.
Esto es coherente con la situación en campo donde los animales más adultos son los que se ven afectados unas semanas antes del sacrificio.
El objetivo del tercer ensayo de vacunación-desafío fue comparar la eficacia contra L. intracellularis de varias pautas de vacunación contra tres de los principales patógenos en cerdos de cebo.
Los resultados obtenidos en los estudios 1 y 2 demuestran un nivel de protección similar a los obtenidos en el estudio 3, lo que indica que los antígenos para PCV y M. hyo no tienen un efecto negativo sobre la eficacia de la vacuna de L. intracellularis.
 En conclusión, en este estudio se demuestra que la vacuna inactivada Porcilis® Lawsonia, sola o mezclada con Porcilis® PCV M Hyo, induce una protección estadísticamente significativa frente a la infección experimental por Lawsonia intracellularis. Esto queda demostrado por la reducción en la sintomatología clínica, la mejora en la ganancia de peso, la menor excreción de Lawsonia intracellularis y la reducción de las puntuaciones de las lesiones macroscópicas y microscópicas en el íleon, cuando se comparan los resultados con los animales del grupo control.
En conclusión, en este estudio se demuestra que la vacuna inactivada Porcilis® Lawsonia, sola o mezclada con Porcilis® PCV M Hyo, induce una protección estadísticamente significativa frente a la infección experimental por Lawsonia intracellularis. Esto queda demostrado por la reducción en la sintomatología clínica, la mejora en la ganancia de peso, la menor excreción de Lawsonia intracellularis y la reducción de las puntuaciones de las lesiones macroscópicas y microscópicas en el íleon, cuando se comparan los resultados con los animales del grupo control.
BIBLIOGRAFÍA
1. Vannucci FA, Gebhart C. Recent advances in understanding the pathogenesis of Lawsonia intracellularis infections. Vet. Pathol. 2014;51:465–77.
2. Lawson GH, Gebhart CJ. Proliferative enteropathy. J. Comp. Pathol. 2000;122:77–100.
3. Jones GF, Ward GE, Murtaugh MP, Rose R, Gephart CJ. Relationship between ileal symbiont intracellularis and porcine proliferative enteritis. Infect. Immun. 1993;61:5237–44.
4. McOrist S, Barcellos DE, Wilson RJ. Global patterns of porcine proliferative enteropathy. Pig J. 2003;51:26–35.
5. Jacobson M, Hård af Segertad C, Gunnasrsson A, Fellström C, de Verdier Klingenberg K, Wallgren P, Jensen-Waern M. Diarrhoea in the growing pig -a comparison of clinical, morphological and microbial findings between animals from good and poor performance herds. Res. Vet. Sci. 2003;74:163–9.
6. Segalés J. Porcine Circovirus type 2 (PCV2) infections: clinical signs, pathology and laboratory diagnosis. Virus Res. 2012;164:10–9.
7. Clark LK, Armstrong CH, Scheidt AB, Van Alstine WG. The effect of Mycoplasma infection on growth in pigs with or without environmental constraints. J. Swine Health Prod. 1993;1:10–4.
8. Haake M, Palzer A, Weissenbacher-Lang Fachinger V, Eggen A, Ritzmann M, Eddicks M. Influence of age on the effectiveness of PCV2 vaccination in piglets with high levels of maternally derived antibodies. Vet. Microbiol. 2014;168:272–80.
9. Agresti A. Categorical Data Analysis. Hoboken, New Jersey, USA: John Wiley & Sons Inc; 2002.
10. Goldsby RA, Kindt TJ, Osborn BA. Kuby Immunology. 4th ed. New York, New York: WH Freeman and Company; 2000. p. 380–410.
11. Guedes MS, Gebhart C. Evidence of cell-mediated immune response and specific local mucosal immunoglobulin (Ig) A production against Lawsonia intracellularis in experimentally infected swine. Can. J. Vet. Res. 2010;74:97–101.
12. Riber U, Heegaard PMH, Corde H, Ståhl M, Jensen TK, Jungersen G. Vaccination of pigs with attenuated Lawsonia intracellularis induced acute phase protein responses and primed cell-mediated immunity without reduction in bacterial shedding after challenge. Vaccine 2015;33:156–62.
13. Roerink F, Morgan CL, Knetter SM, Passat MH, Archibald AL, Ait-Ali T, et al. A novel inactivated vaccine against Lawsonia intracellularis induces rapid induction of humoral immunity, reduction of bacterial shedding and provides robust gut barrier function. Vaccine 2018;36:1500–8.
14. Knight-Jones TJD, Edmont K, Gubbins S, Paton DJ. Veterinary and human vaccine evaluation methods. Proc. R. Soc. B 2014;281:20132839.
Suscribete ahora a la revista técnica porcina
AUTORES

Bioseguridad aplicada frente a Peste Porcina Africana: protocolos clave en granja, logística y control externo
David García Páez
Cómo cuidar la salud respiratoria de los cerdos: medidas clave
Alejandro Cid González Ana I. Pastor Calonge César B. Gutiérrez Martín Mario Delgado García Óscar Mencía-Ares Sonia Martínez Martínez
2026: consolidar fortalezas para avanzar con firmeza

Respuesta de emergencia en accidentes con transporte porcino: la experiencia danesa
Cecilie Kobek-Kjeldager Kirstin Dahl-Pedersen Mette S. Herskin
Microbiota intestinal en el cerdo: de la taxonomía a la función en producción porcina
Eduard de la Torre Candán
Energía neta y crecimiento porcino: claves para una mejor predicción
Gabriela Martínez
La apuesta ganadora de Porgaor, Grupo LANKA: el sistema de alimentación individualizada en maternidades, Materneo de Asserva

El arte de alimentar a cerdas reproductoras: inteligencia artificial al servicio de la nutrición y productividad
Gustavo Márquez Esteban Pablo Fuentes Pardo Sara Crespo Vicente
Lechones más fuertes y numerosos al destete

Estrategia nutricional active feeding en lechones destetados PRRS positivos
Alberto Morillo Alujas
MASTERFLY® BAIT: control eficaz y duradero de moscas

El destete como punto clave de la productividad: puntos críticos a tener en cuenta
Anabel Fernández Bravo Andrea Martínez Martínez Elena Goyena Salgado Emilio José Ruiz Fernández Francisco Frances Diaz José Manuel Pinto Carrasco Manuel Toledo Castillo Simón García Legaz
Medidas para el control de la cepa Rosalía de PRRS

Gestionar la incertidumbre cuando el miedo entra en la granja
Laura Pérez Sala
Bioseguridad y control: estrategias para afrontar el PRRS y PPA en un escenario de riesgo