El papel del microbioma intestinal en el cerdo
La alta prevalencia de Lawsonia intracellularis en las granjas de todo el mundo hace que este patógeno sea el que altere con mayor frecuencia el microbioma intestinal dando oportunidades a otras bacterias.

El cuerpo humano tiene 10 veces más bacterias que células propias. Buena parte de ellas están en el tracto digestivo1, de ahí la importancia de un microbioma intestinal balanceado.
El papel del microbioma intestinal en el cerdo
Se conoce que la composición del microbioma varía entre las diferentes porciones de su tracto intestinal2. Además, este microbioma intestinal influye en la salud global y en el rendimiento productivo de los cerdos, así como en la eficacia en los planes vacunales aplicados a los mismos.
Diversos estudios apuntan que determinadas bacterias, como son Salmonella enterica y Lawsonia intracellularis, pueden alterar la composición del microbioma intestinal3,4.

La alta prevalencia de Lawsonia intracellularis en las granjas de todo el mundo hace que este patógeno sea el que altere con mayor frecuencia el microbioma intestinal dando oportunidades a otras bacterias patógenas.
Es, por tanto, parte y facilitador dentro del complejo entérico porcino. Coinfecciones de Salmonella enterica con Lawsonia intracellularis son un factor de riesgo para el aumento de la diseminación de Salmonella enterica5.

Efecto de la infección por Lawsonia sobre el microbioma
Para comprender mejor la relación de la infección por Lawsonia intracellularis y la comunidad microbiana del intestino, Leite y cols6 evaluaron la respuesta del microbioma del intestino delgado y grueso de cerdos desafiados experimentalmente a las 6 semanas de edad con Lawsonia intracellularis en diferentes etapas de la infección, frente a un grupo control sin desafiar.
La evaluación de la respuesta del microbioma en las diferentes etapas de la infección se llevó a cabo en muestras fecales en el momento de la exposición y se realizó una necropsia secuencial en 6 cerdos por grupo de tratamiento a los 7, 21 y 28 días después de la infección (dpi).
En cada necropsia, las muestras recolectadas para el análisis del microbioma fueron:
![]() Contenido del íleon terminal
Contenido del íleon terminal
![]() Raspado mucoso del íleon terminal
Raspado mucoso del íleon terminal
![]() Contenido cecal
Contenido cecal
![]() Heces
Heces
Después de la extracción de ADN, se realizó un análisis de microbioma analizando la región V4 del gen de ARNr 16S utilizando DADA2 y paquetes phyloseq en R.5. La infección por Lawsonia intracellularis se confirmó mediante:
![]() Realización de inmunohistoquímica (IHC) del tejido intestinal
Realización de inmunohistoquímica (IHC) del tejido intestinal
![]() Medición de la excreción fecal
Medición de la excreción fecal
![]() Seroconversión
Seroconversión
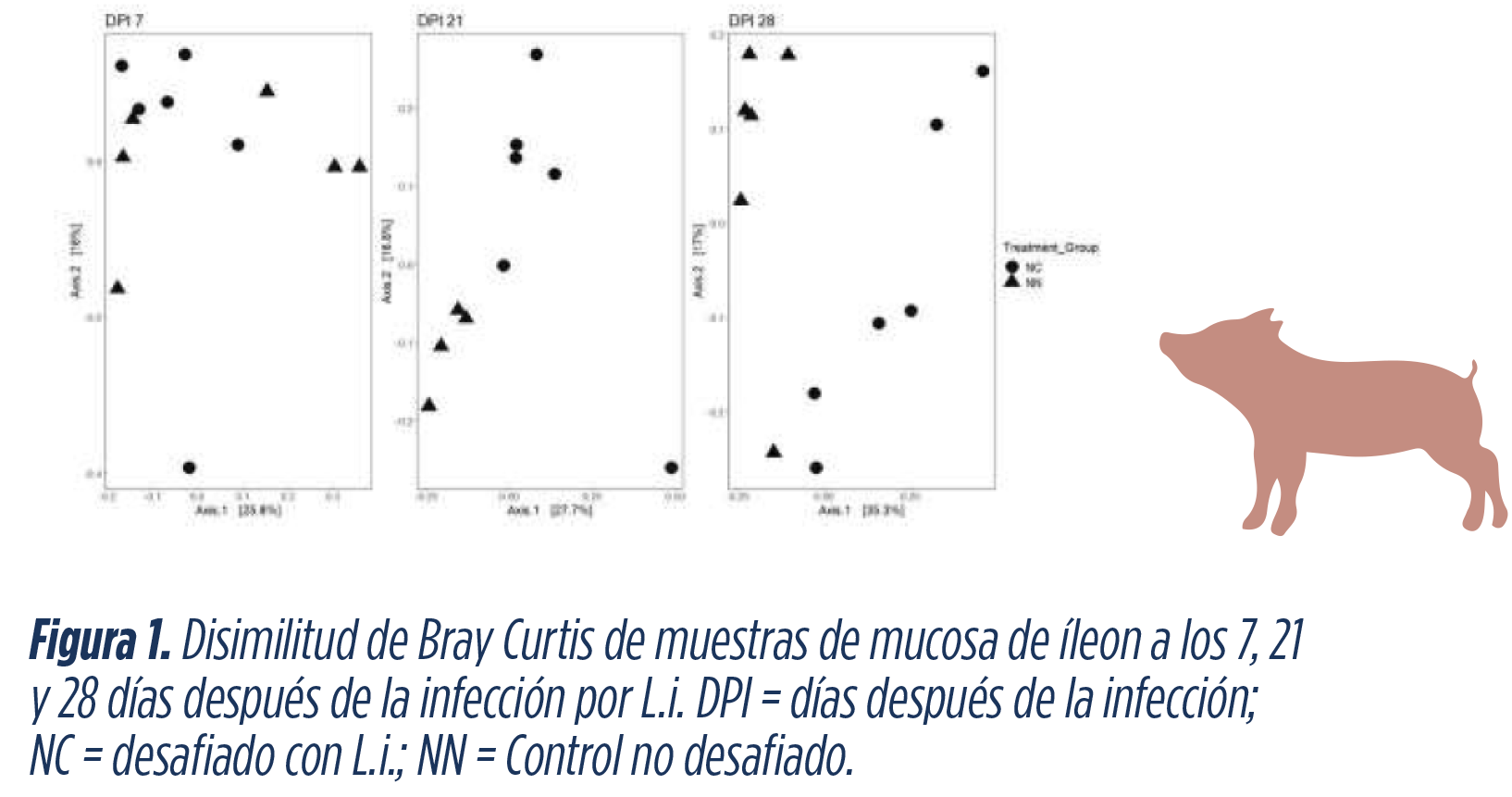
Los resultados de beta diversidad o de diversidad de especies, obtenidos mediante test de disimilitud de Bray Curtis, que cuantifica las diferencias entre dos poblaciones de bacterias (p <0,05), indicaron que la infección por Lawsonia intracellularis provocó un cambio significativo en la composición de la comunidad microbiana del intestino delgado y grueso.

En las muestras de mucosa del íleon, las diferencias entre los tratamientos fueron más evidentes cuando la cantidad de Lawsonia intracellularis aumentaba (7 ppp, p = 0,4, 21 ppp, p = 0,006; 28 ppp, p = 0,003) (Figura 1).
Las bacterias eran significativamente diferentes entre los grupos infectados y no infectados, lo que sugiere que podrían desempeñar un papel en la enfermedad.
Una vez demostrada la alteración del microbioma por la infección de Lawsonia intracellularis, se pasó a evaluar el efecto de la vacunación oral frente a Lawsonia intracellularis y su potencial interacción en la expresión de determinadas bacterias promotoras de enfermedades, que conllevan consecuencias negativas en la salud y en el rendimiento productivo de los animales.
Efecto de la vacunación frente a Lawsonia en la alteración del microbioma y en la excreción de Salmonella
Debido a la asociación entre la infección por Lawsonia intracellularis y Salmonella enterica, Leite y cols7 plantearon la hipótesis de que la vacunación frente a Lawsonia intracellularis disminuiría la diseminación de Salmonella enterica en animales coinfectados.
| Por lo tanto, se convertiría potencialmente en una nueva herramienta para ayudar a controlar la diseminación de Salmonella enterica. |
Por ello, llevaron a cabo un estudio con un total de cinco grupos de tratamiento (Figura 2). Los resultados mostraron cómo la vacunación redujo la eliminación de S. Typhimurium en animales coinfectados en 2,12 log10 organismos por gramo de heces a los 7 días después de la infección.
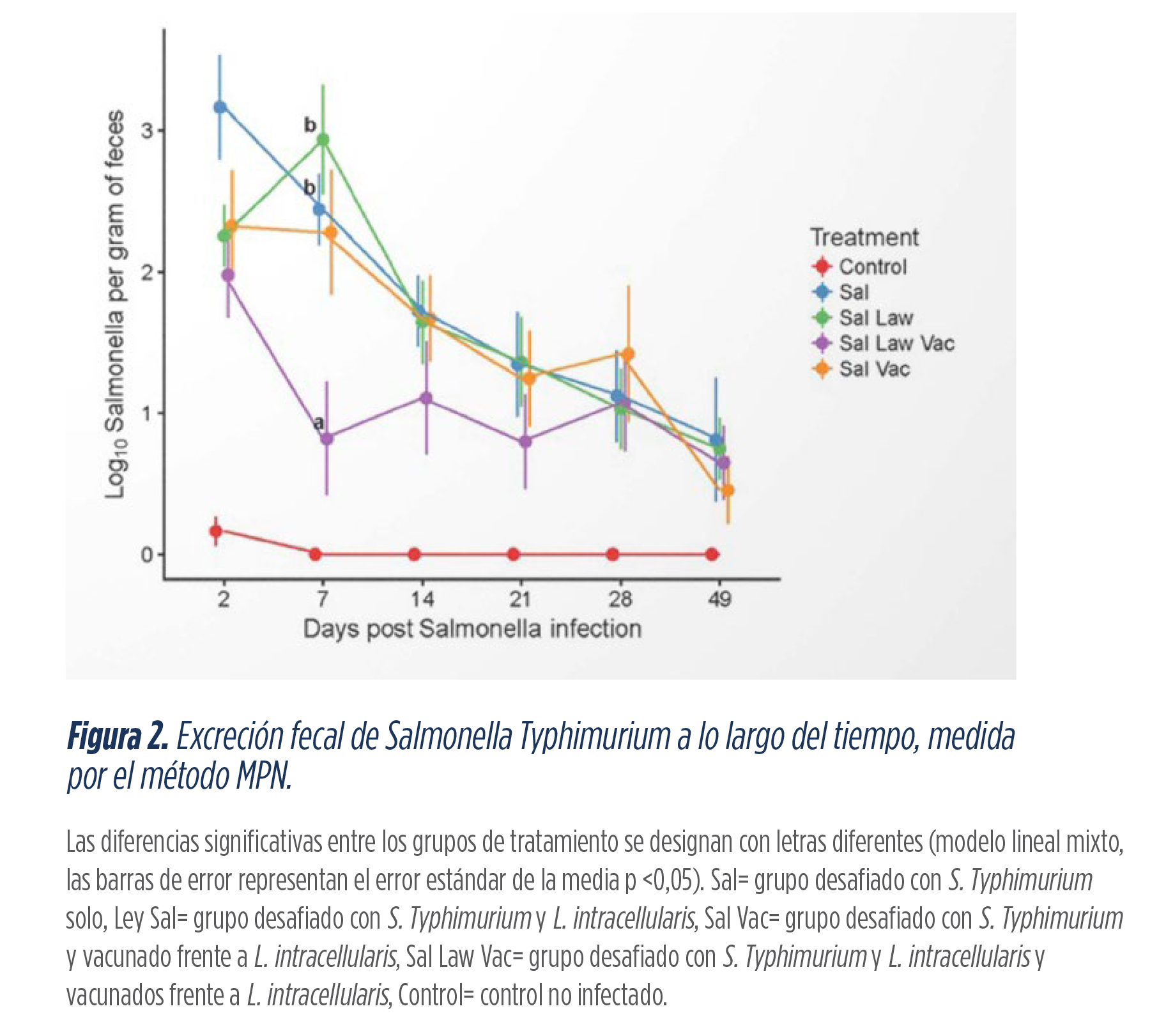
El análisis del microbioma de los distintos grupos de estudio mostró que la vacunación oral frente Lawsonia intracellularis condujo a un aumento en especies de Clostridium, incluido Clostridium butyricum.

Esta bacteria es productora de butirato, un compuesto utilizado en determinadas dietas para la reducción y control de Salmonella. Además, el butirato tiene efecto limitante sobre factores de virulencia (adhesina, LPS y fimbrias) e interviene mejorando y modulando la respuesta inmunitaria innata y adaptativa.
La vacunación oral también redujo las poblaciones de Lactobacillus que se han correlacionado con una mayor virulencia de S. Typhimurium8. Prevotella copri y Collinsella aerofaciens se vieron disminuidas tras la vacunación.
![]() Estas dos especies de bacterias son patobiontes que pueden inducir altas respuestas inflamatorias a nivel intestinal9.
Estas dos especies de bacterias son patobiontes que pueden inducir altas respuestas inflamatorias a nivel intestinal9.
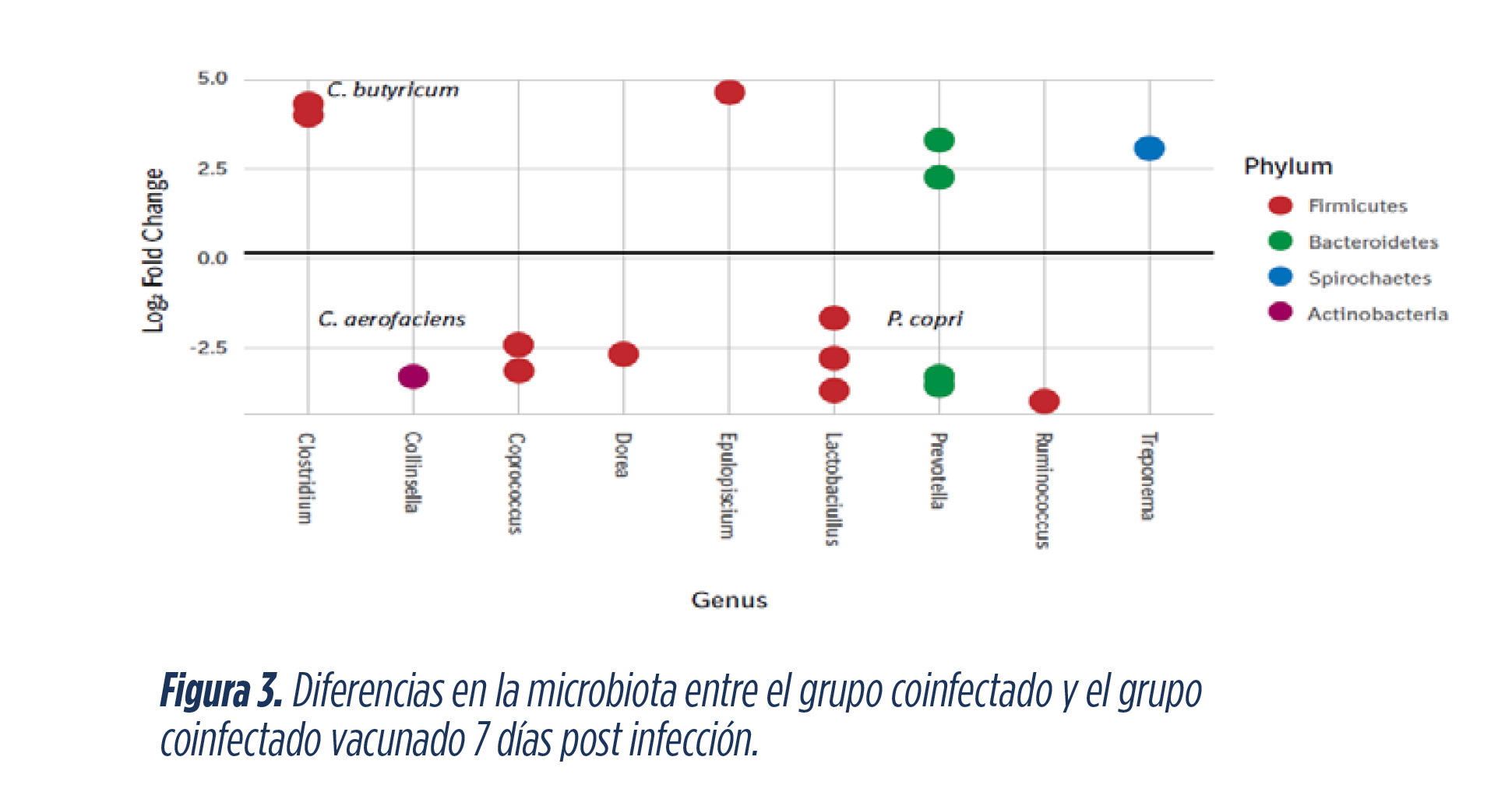
Lawsonia intracellularis forma parte del complejo entérico porcino y su control mediante vacunación oral ha demostrado modificar el microbioma, favoreciendo poblaciones más saludables que confieren protección frente a infecciones por bacterias patógenas.
Conclusiones

Las coinfecciones de Salmonella enterica con Lawsonia intracellularis son un factor de riesgo para el aumento de la diseminación de Salmonella enterica.
Además, la vacunación oral frente a Lawsonia intracellularis puede proporcionar una nueva herramienta para modular la microbiota intestinal, aumentando la cantidad de especies productoras de butirato y disminuyendo la cantidad de Salmonella. De este modo, se incrementa la seguridad alimentaria, al ayudar a prevenir Salmonella enterica y a reducir el uso de antibióticos.
Referencias:
1. Sender, R., et al. (2016). PLoS biology, 14(8).
2. Isaacson R., Kim B. (2012). Anim Health Res Rev.13(1):100-9.
3. Kim, H. y Isaacson, R. (2017). Annu. Rev. Anim. Biosci. 5, 43–63.
4. Borewicz, K. et al. (2015). PLoS One 10, 1–16.
5. Isaacson, R. et al (2011). Conference of Research Workers in Animal Diseases 103.
6. Leite, F., et al. (2018). Scientific reports, 8(1), 1-10.
7. Leite, F. et al. (2021). 12th ESPHM Proceedings
8. Drumo, R. et al. (2016). Frontiers in cellular and infection microbiology, 5, 106.
9. Dillon, et al. (2016). Mucosal immunology, 9(1), 24-37.
Para saber más visita Boehringer Ingelheim
Leer más sobre Boehringer Ingelheim
Suscribete ahora a la revista técnica porcina
AUTORES

Bioseguridad aplicada frente a Peste Porcina Africana: protocolos clave en granja, logística y control externo
David García Páez
Cómo cuidar la salud respiratoria de los cerdos: medidas clave
Alejandro Cid González Ana I. Pastor Calonge César B. Gutiérrez Martín Mario Delgado García Óscar Mencía-Ares Sonia Martínez Martínez
2026: consolidar fortalezas para avanzar con firmeza

Respuesta de emergencia en accidentes con transporte porcino: la experiencia danesa
Cecilie Kobek-Kjeldager Kirstin Dahl-Pedersen Mette S. Herskin
Microbiota intestinal en el cerdo: de la taxonomía a la función en producción porcina
Eduard de la Torre Candán
Energía neta y crecimiento porcino: claves para una mejor predicción
Gabriela Martínez
La apuesta ganadora de Porgaor, Grupo LANKA: el sistema de alimentación individualizada en maternidades, Materneo de Asserva

El arte de alimentar a cerdas reproductoras: inteligencia artificial al servicio de la nutrición y productividad
Gustavo Márquez Esteban Pablo Fuentes Pardo Sara Crespo Vicente
Lechones más fuertes y numerosos al destete

Estrategia nutricional active feeding en lechones destetados PRRS positivos
Alberto Morillo Alujas
MASTERFLY® BAIT: control eficaz y duradero de moscas

El destete como punto clave de la productividad: puntos críticos a tener en cuenta
Anabel Fernández Bravo Andrea Martínez Martínez Elena Goyena Salgado Emilio José Ruiz Fernández Francisco Frances Diaz José Manuel Pinto Carrasco Manuel Toledo Castillo Simón García Legaz
Medidas para el control de la cepa Rosalía de PRRS

Gestionar la incertidumbre cuando el miedo entra en la granja
Laura Pérez Sala
Bioseguridad y control: estrategias para afrontar el PRRS y PPA en un escenario de riesgo