La Figura 1 recoge las muestras más adecuadas para el diagnóstico según la fase de la enfermedad y la evolución de la respuesta inmune, pudiendo emplearse métodos de diagnóstico:
Un diagnóstico ideal de leptospirosis es aquel que llega a establecer la serovariedad implicada . En caso que no pueda llegarse a determinar la serovariedad, es aconsejable al menos determinar a el serogrupo.

La Figura 1 recoge las muestras más adecuadas para el diagnóstico según la fase de la enfermedad y la evolución de la respuesta inmune, pudiendo emplearse métodos de diagnóstico:
Relación entre la respuesta inmune, sintomatología y muestras a enviar para diagnóstico
Figura 1. Evolución de la sintomatología y título de anticuerpos durante la leptospirosis.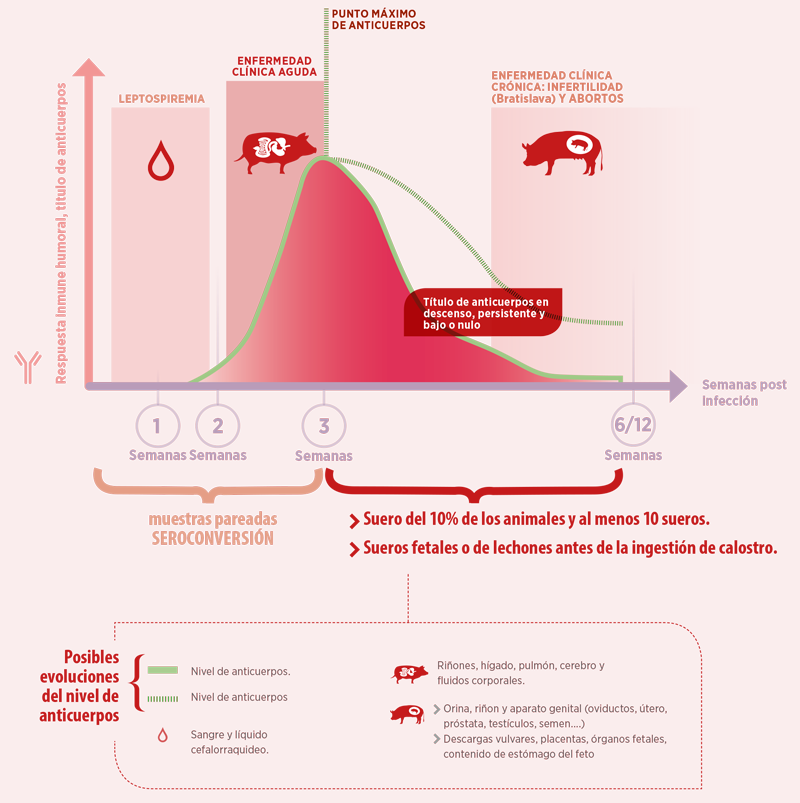
Métodos directos

El único método que nos permite determinar la serovariedad de Leptospira es el cultivo y aislamiento, pero es difícil, caro y tedioso.
Condiciones de envío de la muestra





Entre los métodos de diagnóstico directo de la leptospirosis más utilizados están las técnicas de PCR debido a las ventajas que ofrecen:
Las pruebas más utilizadas son las dirigidas a genes presentes únicamente en las leptospiras patógenas, por lo que un resultado positivo solo indica, en este caso, la presencia de una cepa patógena pero no permite la identificación directa de la serovariedad.



Interpretación de resultados de los métodos de diagnóstico directo



MÉTODOS INDIRECTOS
PRUEBA DE MICROAGLUTINACIÓN (MAT)
La prueba más utilizada para el diagnóstico de leptospirosis es la prueba de microaglutinación (microscopic agglutination test o MAT).
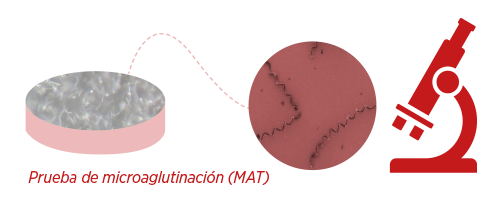
 La prueba consiste en mezclar diferentes diluciones del suero con una suspensión de leptospiras vivas y el título será la dilución más alta en la que se observen la mitad o más de las leptospiras aglutinadas.
La prueba consiste en mezclar diferentes diluciones del suero con una suspensión de leptospiras vivas y el título será la dilución más alta en la que se observen la mitad o más de las leptospiras aglutinadas.
Se considera significativo un título de 1/100 o mayor.
ESPECIFICIDAD DE LA PRUEBA DE MICROAGLUTINACIÓN
La prueba de microaglutinación es serogrupo específica y relativamente serovariedad específica. Es importante elegir las serovariedades representativas de cada serogrupo que se incluyen en la prueba
En nuestro país deberían incluirse como mínimo cepas de las serovariedades Bratislava, Canicola, Icterohaemorrhagiae, Pomona y Castellonis.


Como prueba individual, tiene valor diagnóstico en los casos agudos.



El diagnóstico se hará viendo si hay seroconversión, tomando un suero en la fase aguda y otro 2-3 semanas más tarde

En casos de abortos y nacidos muertos o poco viables tiene valor diagnóstico si se detectan anticuerpos en suero fetal o en suero de lechones que no han tomado calostro.




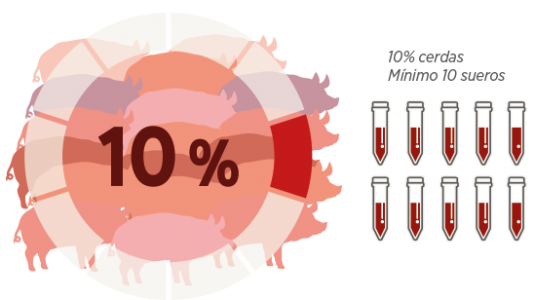
En estos casos, se enviará al laboratorio suero de al menos un 10% de las cerdas, distribuidos proporcionalmente por ciclos y enviando siempre un mínimo de 10 sueros, para determinar si ha habido infección por estas serovariedades en la granja.

Por último, el MAT no es fiable para la detección de portadores renales (serovariedades Pomona Tarassovi, Bratislava y Muenchen) y/o genitales (serovariedades Bratislava y Muenchen).
Así, se han descrito casos de infecciones por la serovariedad Pomona en los que la leptospiruria dura años, por lo que en estos animales no detectaremos títulos significativos de anticuerpos, pero estarán eliminando leptospiras en la orina.


En general, la cepa frente a la que se obtengan los títulos más altos en la MAT se corresponderá con el serogrupo infectante. Sin embargo hay que considerar varios aspectos:
Ej.: la serovariedad que se aconseja como representativa del serogrupo Pomona es la serovariedad Pomona. Si en el MAT se obtienen los títulos más altos frente a esta cepa, no diferencia si la serovariedad implicada es la serovariedad adaptada Pomona o la serovariedad accidental Mozdok, que son las dos que sabemos que circulan en nuestro país de este serogrupo.
Ej.: en caso de infecciones por el serogrupo Pomona, hemos observado títulos en un mismo suero de 1/10.000 tanto frente a la serovariedad Pomona como a la serovariedad Bratislava o diferencias en el título frente a ambas serovariedades de solo una dilución.

Finalmente, las pruebas ELISA son muy útiles por su sencillez en comparación con el MAT.
El problema de las pruebas ELISA es que normalmente se han validado frente al MAT tomando como punto de corte el título de 1/100, por lo que no son de gran utilidad para detección de portadores, y al igual que el MAT, no diferencian animales infectados de vacunados.

Suscribete ahora a la revista técnica porcina
AUTORES

Bioseguridad aplicada frente a Peste Porcina Africana: protocolos clave en granja, logística y control externo
David García Páez
Cómo cuidar la salud respiratoria de los cerdos: medidas clave
Alejandro Cid González Ana I. Pastor Calonge César B. Gutiérrez Martín Mario Delgado García Óscar Mencía-Ares Sonia Martínez Martínez
2026: consolidar fortalezas para avanzar con firmeza

Respuesta de emergencia en accidentes con transporte porcino: la experiencia danesa
Cecilie Kobek-Kjeldager Kirstin Dahl-Pedersen Mette S. Herskin
Microbiota intestinal en el cerdo: de la taxonomía a la función en producción porcina
Eduard de la Torre Candán
Energía neta y crecimiento porcino: claves para una mejor predicción
Gabriela Martínez
La apuesta ganadora de Porgaor, Grupo LANKA: el sistema de alimentación individualizada en maternidades, Materneo de Asserva

El arte de alimentar a cerdas reproductoras: inteligencia artificial al servicio de la nutrición y productividad
Gustavo Márquez Esteban Pablo Fuentes Pardo Sara Crespo Vicente
Lechones más fuertes y numerosos al destete

Estrategia nutricional active feeding en lechones destetados PRRS positivos
Alberto Morillo Alujas
MASTERFLY® BAIT: control eficaz y duradero de moscas

El destete como punto clave de la productividad: puntos críticos a tener en cuenta
Anabel Fernández Bravo Andrea Martínez Martínez Elena Goyena Salgado Emilio José Ruiz Fernández Francisco Frances Diaz José Manuel Pinto Carrasco Manuel Toledo Castillo Simón García Legaz
Medidas para el control de la cepa Rosalía de PRRS

Gestionar la incertidumbre cuando el miedo entra en la granja
Laura Pérez Sala
Bioseguridad y control: estrategias para afrontar el PRRS y PPA en un escenario de riesgo